 更多“间歇反应器的物料衡算方程式为()。”相关的问题
更多“间歇反应器的物料衡算方程式为()。”相关的问题
第2题
液相可逆反应速率方程的求取 一级液相可逆反应AP,cA0=0.5mol/L,cP0=0,间歇反应器中进行反应。8min后,A的转
液相可逆反应速率方程的求取
一级液相可逆反应A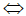 P,cA0=0.5mol/L,cP0=0,间歇反应器中进行反应。8min后,A的转化率为33.3%,平衡转化率为66.7%,求该反应的速率方程式。
P,cA0=0.5mol/L,cP0=0,间歇反应器中进行反应。8min后,A的转化率为33.3%,平衡转化率为66.7%,求该反应的速率方程式。
第4题
反应速率方程式的求取 在等温间歇反应器中进行如下液相反应: A+B→R+P 实验数据如表所示: cA0=0.307kmol
反应速率方程式的求取
在等温间歇反应器中进行如下液相反应:
A+B→R+P
实验数据如表所示:
cA0=0.307kmol/m3,cB0=0.585kmol/m3
t(h) | 0 | 1.15 | 2.90 | 5.35 | 8.70 |
cA(kmol/m3) | 0.307 | 0.211 | 0.130 | 0.073 | 0.038 |
求反应动力学方程。
第5题
在脱硫装置的化工设计热量衡算中,以下()不是热量衡算步骤。
A.确定热量衡算的步骤,收集物性数据、操作条件数据、热性质数据
B.选择衡算的计算基准和能量基准,列出各种关系式、包括热量衡算式、焓方程式及物料衡算方程式
C.将计算结果整理列成热量平分表,并进行验算。
D.计算总热量
第6题
在反应体积为2.5m3的理想间歇反应器(IBR)中,维持反应温度为348K进行如下液相反应:A+B→P 实验测得反应速率
在反应体积为2.5m3的理想间歇反应器(IBR)中,维持反应温度为348K进行如下液相反应:A+B→P
实验测得反应速率方程式为-rA=kcAcBmol·L-1·s-1,k=2.78×10-3L·mol-1·s-1。当反应物A、B的初始浓度CA,0=CB,0=4mol·L-1,而转化率xA=80%时,该IBR平均每分钟可处理0.684kmol的反应物A。
若将反应置于一个管径为125mm的PFR中进行,反应温度不变,且处理量和要求转化率相同,试求所需PFR的长度为多少?
第7题
间歇反应器,亦称间歇式全混槽(釜),间歇搅拌槽(釜)等,其基本特征是:()。
A.其中的化学变化仅与热变化有关
B.其中的化学变化和热变化仅与时间有关
C.反应器内物料的浓度和温度是位置的函数,与时间无关
D.反应器内物料的浓度和温度是时间的函数,与位置无关


 如果结果不匹配,请
如果结果不匹配,请 

















