 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
电势滴定时,由于在计量点附近离子浓度发生______,引起指示电极的______发生突跃,故测量工作电池的______变
化,就可确定滴定的______。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“电势滴定时,由于在计量点附近离子浓度发生______,引起指…”相关的问题
更多“电势滴定时,由于在计量点附近离子浓度发生______,引起指…”相关的问题
有一三元酸,其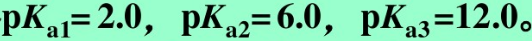 用氢氧化钠溶液滴定时,第一和第二化学计量点的pH分别为多少?两个化学计量点附近有无pH突跃?可选用什么指示剂?能否直接滴定至酸的质子全部被作用?
用氢氧化钠溶液滴定时,第一和第二化学计量点的pH分别为多少?两个化学计量点附近有无pH突跃?可选用什么指示剂?能否直接滴定至酸的质子全部被作用?
A.溶液的pH值太高
B.被滴定物浓度太小
C.指示剂变色范围太宽
D.反应产物的副反应严重
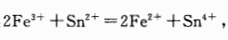 下列叙述正确的是()。
下列叙述正确的是()。A.滴定曲线对称
B. 滴定曲线不对称,计量点的电势偏向 Sn4+ /Sn2+ 电对一方
C.滴定曲线不对称,计量点的电势偏向Fe3+ /Fe2+电对一方
D. 突跃大小与反应物的初始浓度有关
A.滴定曲线对称
B. 滴定曲线不对称,计量点的电势偏向Sn4+/Sn2+电对一方
C. 滴定曲线不对称,计量点的电势偏向Fe3+/Fe2+电对一方
D. 突跃大小与反应物的初始浓度有关
A.lgKNY-lgKMY≥2和IgCK'MY和IgCK'NY≥6
B.IgKNY-lgKMY≥5和IgCK'MY和IgCK'NY≥3
C.IgKNY-IgKMY≥8和IgCK'MY和IgCKNY≥4