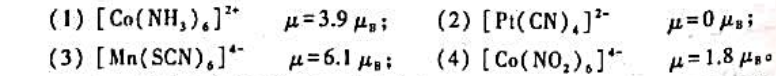更多“下列化合物中的氧原子的杂化方式与其他几个不同的是()”相关的问题
更多“下列化合物中的氧原子的杂化方式与其他几个不同的是()”相关的问题
第1题
下列关于碳族元素说法错误的是()。
A.碳族元素基态原子的价电子层结构为ns2np2
B.锡的金属性质比锗强,可以与非氧化性的酸反应
C.碳酸盐的热稳定性不高主要取决于碳原子的杂化方式
D.硅酸是二元酸,比碳酸还弱
第4题
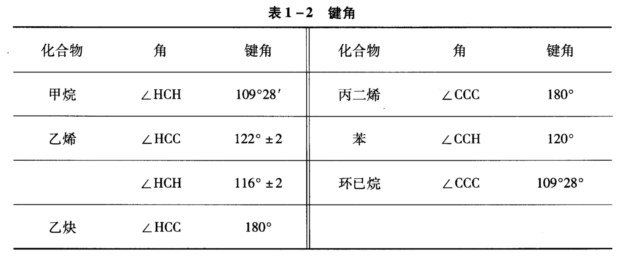
结合表1—2中的数据回答下列问题: (i)哪些化合物分子中的原子都在同一平面中? (ii)哪些
结合表1—2中的数据回答下列问题: (i)哪些化合物分子中的原子都在同一平面中? (ii)哪些化合物分子中的原子都在一条直线上? (iii)哪些化合物分子中的原子处在两个相互垂直的平面中? (iv)哪些化合物分子中的碳原子都是sp3杂化轨道?
第5题
配位化合物形成时中心离子(或原子)轨道杂化成键,与简单二元化合物形成时中心原子轨道杂化成键的主要不同之处是:配位化合物形成时中心原子的轨道杂化()。
A.一定要有 d 轨道参与杂化;
B.一定要激发成对电子成单后杂化;
C.一定要有空轨道参与杂化;
D.一定要未成对电子偶合后让出空轨道杂化。
第7题
关于杂化轨道理论,下列说法错误的是()。
关于杂化轨道理论,下列说法错误的是()。
点击查看答案
A、杂化轨道是由不同原子的价层能量相近的原子轨道组合而成
B、有几个原子轨道参加杂化,就形成几个杂化轨道
C、杂化轨道比杂化前的原子轨道成键能力强
D、不同类型的杂化轨道间的夹角不同
第9题
有关羰基的描述正确的是
A.羰基中的碳原子为sp2杂化
B.羰基中π电子云偏向于氧原子一边
C.羰基碳氧双键是由一个σ键和一个π键组成
D.羰基的加成属于亲核加成
E.羰基碳原子带有部分正电荷,而氧原子则带有部分负电荷


 如果结果不匹配,请
如果结果不匹配,请