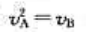题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
若基元反应A=2Z的活化能为Ea,而其逆反应的活化能为Ea’。 (1)加入催化剂后,各有何变化? (2)
若基元反应A=2Z的活化能为Ea,而其逆反应的活化能为Ea’。
(1)加入催化剂后,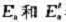 各有何变化?
各有何变化?
(2)加入不同的催化剂,对Ea的影响是否相同?
(3)改变A的起始浓度,Ea有何变化?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
若基元反应A=2Z的活化能为Ea,而其逆反应的活化能为Ea’。
(1)加入催化剂后,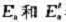 各有何变化?
各有何变化?
(2)加入不同的催化剂,对Ea的影响是否相同?
(3)改变A的起始浓度,Ea有何变化?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“若基元反应A=2Z的活化能为Ea,而其逆反应的活化能为Ea’…”相关的问题
更多“若基元反应A=2Z的活化能为Ea,而其逆反应的活化能为Ea’…”相关的问题
A.正反应的活化能与逆反应的活化能相等
B.正反应的活化能大于逆反应的活化能
C.逆反应的活化能大于正反应的活化能
D.无法比较正、逆反应的活化能的相对大小
反应A-Y+Z是吸热反应,正反应的活化能为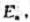 逆反应的活化能为
逆反应的活化能为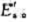 则正反应的活化能与逆反应的活化能之间的关系为()。
则正反应的活化能与逆反应的活化能之间的关系为()。
A、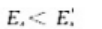
B、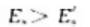
C、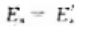
D、三种都有可能
已知在管式反应器中进行液相反应:
A→R+S
其为吸热反应,反应管外油浴温度(Tc)恒定为613K,假定已知其管内温度(T)与反应物的转化率(xA)的关系为

式中,速率常数
若反应器入口温度为613K,反应器出口转化率为90%,试列表计算转化率每变化0.1,管式反应器内相应的温度。
根据实验,在一定范围内,NO和Cl2的基元反应方程式可用下式表示:
2NO+Cl2→2NOCl
对基元反应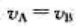 反应物A的消耗速率vA与反应物B的消耗速率vB的关系为()
反应物A的消耗速率vA与反应物B的消耗速率vB的关系为()
A、
B、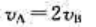
C、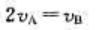
D、