 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
反应
反应 已达到化学平衡状态,若升高温度,生成物C的浓度增加,则逆反应是( )
已达到化学平衡状态,若升高温度,生成物C的浓度增加,则逆反应是( )
A.放热反应
B.吸热反应
C.没有明显的热效应
D.无法判断
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 已达到化学平衡状态,若升高温度,生成物C的浓度增加,则逆反应是( )
已达到化学平衡状态,若升高温度,生成物C的浓度增加,则逆反应是( )A.放热反应
B.吸热反应
C.没有明显的热效应
D.无法判断
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“反应已达到化学平衡状态,若升高温度,生成物C的浓度增加,则逆…”相关的问题
更多“反应已达到化学平衡状态,若升高温度,生成物C的浓度增加,则逆…”相关的问题
已知可逆反应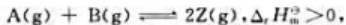 在温度T时达到了化学平衡。若采取下列措施,可能使化学平衡向正反应方向移动的是()。
在温度T时达到了化学平衡。若采取下列措施,可能使化学平衡向正反应方向移动的是()。
A、保持原来的温度
B、升高温度
C、降低温度
D、压缩系统的体积,以增大总压力
A.反应物浓度,放热,放热,吸热
B.反应物浓度,吸热,吸热,放热
C.反应的热效应,吸热,放热,吸热
D.反应的热效应,吸热,吸热,放热
A.可逆反应的特征是正反应速率和逆反应速率相等
B.在其它条件不变时,升高温度可以使化学平衡向放热反应的方向移动
C.在其它条件不变时,增大压强一定会破坏气体反应的平衡状态
D.在其它条件不变时,使用催化剂可改变化学反应速率,但不能改变化学平衡状态
A.混合气体的密度不再变化
B.反应容器中Y的质量分数不变
C.X的分解速率与Y的消耗速率相等
D.单位时间内生成1molY的同时生成2molX
A.容器内的压强不再改变
B.(SO2):c(O2):c(SO3)=2:1:2
C.混合气体的密度不再改变
D.SO2的生成速率与SO3的消耗速率相等
A.N2、H2完全转化为NH3
B.N2、H2、NH3在容器中共存
C.反应已达到化学平衡状态
D.N2、H2、NH3的浓度不再改变
A.升高温度可使化学平衡向正反应方向移动
B.#图片1$#
C.反应物的分压等于生成物的分压
D.加入催化剂,可使化学平衡向正反应方向移动
对于反应N2(g)+3H2(g)=2NH3(g),△H<0。则升高温度,化学平衡 __________ 移动;减小总压,化学平衡__________移动;加入氮气,化学平衡___________移动;加入氢气,H2(g)的平衡分压_________;