 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
300K时,合成氨反应:的温度范围内保持不变,计算该可逆反应在600K时的标准平衡常数。
300K时,合成氨反应: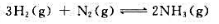 的温度范围内保持不变,计算该可逆反应在600K时的标准平衡常数。
的温度范围内保持不变,计算该可逆反应在600K时的标准平衡常数。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
300K时,合成氨反应: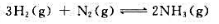 的温度范围内保持不变,计算该可逆反应在600K时的标准平衡常数。
的温度范围内保持不变,计算该可逆反应在600K时的标准平衡常数。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“300K时,合成氨反应:的温度范围内保持不变,计算该可逆反应…”相关的问题
更多“300K时,合成氨反应:的温度范围内保持不变,计算该可逆反应…”相关的问题
合成氨反应N2(g)+3H2(g)
 2NH3(g)达平衡后加惰性气体,且保持体系温度,总压不变。(气体为理想气体)。则()
2NH3(g)达平衡后加惰性气体,且保持体系温度,总压不变。(气体为理想气体)。则()

合成氨反应:

在30.4MPa,500℃时,K为7.8×10-5,计算该温度时下列反应的K:
A.-74.66
B.74.66
C.5.75
D.-5
某对行反应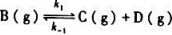 在300K时,k1=10s-1,k-1,=100Pa-1.s-1.当温度升高10°C时k1与k-1均增大一倍,则正、逆反应的活化能
在300K时,k1=10s-1,k-1,=100Pa-1.s-1.当温度升高10°C时k1与k-1均增大一倍,则正、逆反应的活化能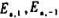 及反应的
及反应的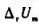 为().
为().
A.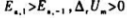
B.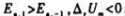
C.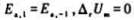
D.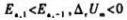
已知合成氨反应 N2(g)+3H2(g)=2NH3(g) 在298K、pθ下的△rGmθ=-33.26kJ.mol-1,△rGmθ=-92.38kJ.mol-1,假设此反应的△rGmθ不随T而变化,求500K时此反应的△rGmθ,并由计算结果说明温度对反应的影响。
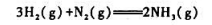
A.升高温度使吉布斯自由能变和和标准吉布斯自由能变均增大
B.升高温度可以使平衡向右移动
C.升高温度可以使平衡常数增大
D.正反应自发时,随着反应进行,N2和H2分压逐渐减小,NH3分压逐渐增大,所以平衡常数Kp逐渐增大