 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
生物碱的沉淀反应要求在以下何种溶液中进行()。
A.碱性溶液
B.中性有机溶剂
C.水
D.碱性有机溶剂
E.酸性溶液
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.碱性溶液
B.中性有机溶剂
C.水
D.碱性有机溶剂
E.酸性溶液
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“生物碱的沉淀反应要求在以下何种溶液中进行()。”相关的问题
更多“生物碱的沉淀反应要求在以下何种溶液中进行()。”相关的问题
A.一般在稀酸水溶液中进行
B.可应用于生物碱的分离纯化
C.选用一种沉淀试剂反应呈阳性,即可判断有生物碱
D.有些沉淀试剂可用作纸色谱和薄层色谱的显色剂
E.可不必处理酸水提取液
A.化学鉴别最常用的是沉淀反应和显色反应
B.紫外吸收光谱较红外吸收光谱丰富,是更好的药物鉴别方法
C.生物碱可用生物碱沉淀试剂反应来进行鉴别
D.在生物碱类药物分子中,大都含有双键结构,因此具有紫外特征吸收峰,据此用于鉴别
由△Gθ-T图,讨论下列问题:
将Cu(N03)2缓慢滴人NH4HCO3溶液中(倒滴法),反应初期不见沉淀析出,为什么?随着Cu(NO3)2的不断加入发现有沉淀产生,试判断是何种沉淀。写出有关的离子反应方程式。
用生物碱试剂沉淀蛋白质
A.将生物碱试剂直接加入溶液中
B.先向溶液中加碱
C.先向溶液中加酸
D.使溶液的pH≥pI
E.使溶液pH>pI
阅读下列三段材料,根据要求完成任务。
材料一《普通高中化学课程标准(实验)》关于“难溶电解质的溶解平衡”的内容标准是:能描述沉淀溶解平衡,知道沉淀转化的本质。
材料二某版本高中实验教科书《化学4》“难溶电解质的溶解平衡”的部分内容:
二、沉淀反应的应用
难溶电解质的溶解平衡也是动态平衡.同样可以通过改变条件使平衡移动——溶液中的离子转化为沉淀,或沉淀转化为溶液中的离子。
1.沉淀的生成
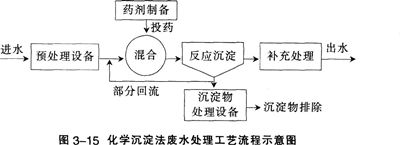
在涉及无机制备、提纯工艺的生产、科研、废水处理等领域中.常利用生成沉淀来达到分离或除去某些离子的目的。例如,工业原料氯化铵中含杂质氯化铁,使其溶解于水,再加入氨水调节pH至7~8,可使Fe3+生成Fe(OH)3沉淀而除去。除调节pH使生成氢氧化物沉淀外,以Na2s、H2s等作沉淀剂,使某些金属离子如Cu2+、Hg2+等,生成极难溶的硫化物CuS、HgS等沉淀,也是分离、除去杂质常用的方法。 .
思考与交流
利用生成沉淀分离或除去某种离子,首先要使生成沉淀的反应能够发生:其次希望沉淀生成的反应进行得越完全越好。
1.如果要除去某溶液中的S042-你选择加入钙盐还是钡盐?为什么?
2.以你现有的知识,你认为判断沉淀能否生成可从哪些方面考虑?是否可能使要除去的离子全部通过沉淀除去?说明原因。
材料三教学对象为高中二年级学生,他们已经学习了必修化学1、必修化学2和“化学反应与能量”“化学反应速率和化学平衡”以及“弱电解质的电离”“水的电离和溶液的酸碱度”“盐类的水解”等知识。
要求:
(1)回答材料二中“思考与交流”中的问题。
(2)完成“难溶电解质的溶解平衡”的教学设计,内容包括教学重难点、教学方法和教学过程。
A.醇与钠反应没有水与钠反应剧烈
B.乙醇与浓硫酸140℃发生分子内脱水
C.在苯酚溶液中滴入FeCl3溶液呈紫色
D.在苯酚稀溶液中滴入溴水可出现白色沉淀
已知反应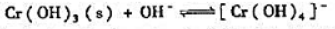 的标准平衡常数
的标准平衡常数
Kθ=10-0.40.在1.0L0.10mol.L-1Cr3+溶液中,当Cr(OH)3沉淀完全时,溶液的pH是多少?要使沉淀出的Cr(OH)3刚好在1.0LNaOH溶液中完全溶解并生成[Cr(OH)4]-,问落被中的c(OH)是多少?并求[Cr(OH)4]-的标准稳定常数.