 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
写出Ca(OH)2(s)与氯化镁溶液反应的离子方程式,计算该反应在298K下的标准平衡常数Kθ如果CaCl2溶液中含有少量MgCl可怎样除去?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“写出Ca(OH)2(s)与氯化镁溶液反应的离子方程式,计算该…”相关的问题
更多“写出Ca(OH)2(s)与氯化镁溶液反应的离子方程式,计算该…”相关的问题
0ml.的烧瓶中,温度为25℃,压力为27.9kPa.使该气体通入Ca(OH)2饱和溶液中得到白色固体C.如果将少量B加入水中,所得B溶液能使红色石蕊试纸变蓝.B的水溶液被盐酸中和后,经蒸发干燥得白色固体D.用D做焰色反应试验,火焰为绿色.如果B的水溶液与H2SO4反应后,得到白色沉淀E,E不溶解于盐酸.试确定A、B、C、D、E各为什么物质,并写出相关反应方程式.
A.活性SiO2和Al2O3与C3S ;
B.活性SiO2和Al2O3与Ca(OH)2;
C.二次反应促进了熟料水化
D.(b+c)
已知298K时,Ca(OH)2(s)的 =-897.5kJ·mol-1,H2O(1)的
=-897.5kJ·mol-1,H2O(1)的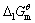 =-237.1kJ·mol-1,
=-237.1kJ·mol-1,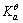 = 1.00×10-7,试求电对Ca(OH)2/Ca的电极电势。
= 1.00×10-7,试求电对Ca(OH)2/Ca的电极电势。
(OH)2的标准溶度积常数 为()。
为()。
A、5.0×10-7
B、2.0X10-6
C、4.0×10-6
D、8.0X10-6
A.0.02~0.05mol/LHCl
B.2%NaOH水溶液
C.3%~5%HCl
D.NaHCO3水溶液
E.Ca(OH)2溶液
在ZnSO4溶液中慢慢加入NaOH溶液,可生成白色Zn(OH)2沉淀。把沉淀分成三份,分别加入HCl溶液、过量的NaOH溶液及氨水,沉淀都能溶解。写出三个反应式。