 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
对H2(g)+I2(g)=2HI(g)的反应,下列哪一措施将改变平衡常数值()。
A.升高温度
B.使用较小的反应容器
C.加更多的H2
D.除去一些HI
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.升高温度
B.使用较小的反应容器
C.加更多的H2
D.除去一些HI
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“对H2(g)+I2(g)=2HI(g)的反应,下列哪一措施将…”相关的问题
更多“对H2(g)+I2(g)=2HI(g)的反应,下列哪一措施将…”相关的问题
氯气和碘蒸气反应用下列反应式表示;.
H2(g)+I2(g)=2HI(g)
在713.15K,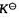 =50.0。如用下列反应式表示时:
=50.0。如用下列反应式表示时:

计算713.15K时它们的平衡常数 。
A.239.2kJ
B.438.4kJ
C.119.6kJ
D.358.8kJ
℃下,每升气体会产生3.5×1029次·s-1的碰撞,如果每次碰撞都会发生化学反应,试计算HI的分解反应的速率.实验测定,该反应实际的反应速率是1.2×10-8·mol·dm-3·s-1,试求HI气体中活化分子的百分数(设每次活化分子的相互碰撞都产生反应).
A.CO2(g)+CaO(s)→CaCO3(S)
B.1/2H2(g)+1/2I2(g)→HI(g)
C.H2(g)+Cl2(g)→2HCl(g)
D.H2(g)+1/2O2(g)→H20(g)
已知晶体碘I2(s)和碘蒸气I2(g)的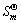 分别为116.1J·mol-1·K-1和260.7J·mol-1·K-1,碘蒸气的
分别为116.1J·mol-1·K-1和260.7J·mol-1·K-1,碘蒸气的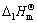 为62.4kJ·mol-1,试计算晶体碘的正常升华温度。
为62.4kJ·mol-1,试计算晶体碘的正常升华温度。
(1)写出H2(g),CO(g),CH3OH(I)燃烧反应的热化学方程式;
(2)甲醉的合成反应为:CO(g)+2H2(g)→CH3OH(l).
利用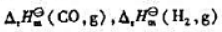
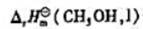 计算该反应的
计算该反应的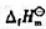 .
.