 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
指出下列分子或离子的几何构型键角、中心原子的杂化轨道,并估计分子中键的极性.(1)KrF2(2)BF4-(3)SO3(4)XeF4(5)PCl5(6)SeF6
指出下列分子或离子的几何构型键角、中心原子的杂化轨道,并估计分子中键的极性.(1)KrF2(2)BF4-(3)SO3(4)XeF4(5)PCl5(6)SeF6
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“指出下列分子或离子的几何构型键角、中心原子的杂化轨道,并估计…”相关的问题
更多“指出下列分子或离子的几何构型键角、中心原子的杂化轨道,并估计…”相关的问题
下列各对分子或离子中何者具有相同的几何构型?
(1)SF4与CH4;(2)CIO2与H2O;(3)CO2与BeH2;
(4)NO2+与NO2;(5)PCI4+与SO42-;(6)BrF5与XcOF4.
试用价层电子对互斥理论判断下列分子或离子的空间构型,再用杂化轨道理论说明它们的成键情况。
(1)SF3; (2)BeF3; (3)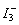 ; (4)
; (4)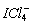 ;
;
A.原子轨道的杂化,只有在形成分子的过程中才会发生,而孤立的原子是不可能发生杂化的
B.只有能量相近的原子轨道才能发生杂化
C.一定数目的原子轨道杂化后,可以得到更多数量的杂化轨道
D.CH4分子中有四个能量相等的C—H键,键角为109°28′,分子的空间构型为正四面体,这一情况可以用杂化轨道理论解释
根据下列分子偶极矩数据,判断分子的极性和几何构型。
SiCl4(μ=0),CH3Cl(μ=6.38×10-30C·m),SO3(μ=0),BCl3(μ=0),PCl3(μ=2.6×10-30C·m)。