 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
3 mol温度为273K的理想气体,先经等温过程使体积膨胀到原来的5倍,然后等容加热,使其末态压强恰好等于初态的压强,整个过程传给气体的热量为8×104J.画出此过程的p- V图,并求出气体的比热容比γ= Cp/Cv之值(摩尔气体常量R =8.31J·mol·K-1).
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“3 mol温度为273K的理想气体,先经等温过程使体积膨胀到…”相关的问题
更多“3 mol温度为273K的理想气体,先经等温过程使体积膨胀到…”相关的问题
设有压力为100kPa、温度为293K的理想气体3dm3,在等压下加热,直到最后温度为353K为止。计算过程中的W、△U、△H和Q。已知该气体的等压摩尔热容Cp,m=(27.28+3.26×10-3T/K)J·mol·K-1。
一个绝热活塞把刚性绝热密封气缸分成A和B两部分,A室与B室内装有同种理想气体。其Cp,m=29.184J/(mol·K)。活塞面积为0.1m2,气缸长度为0.3m。初始时A室占(1/3V),PA1=400K;PB1=0.2MPa,TA1=300K,活塞两侧的压力差与通过活塞杆上作用的外力F保持平衡。外力F缓慢减小,直至两室压力相等,此时测得A室内温度为354.6 K。若活塞与缸壁之间无摩擦,求终态时两室压力、温度和系统对外力作的功。
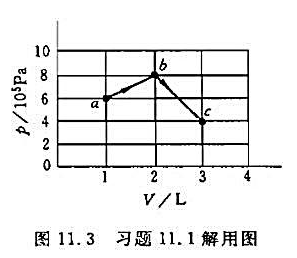
1 mol氧气(当成刚性分子理想气体)经历如图11.3 所示的过程由a经b到c。求在此过程中气体对外做的功、吸的热以及熵变。
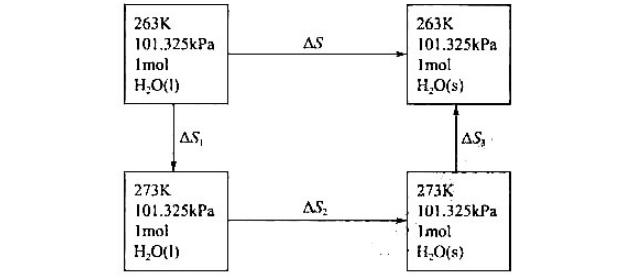
将压力为0.1MPa,温度为0℃,相对湿度为60%的湿空气经多变压缩(n=1.25)至60℃,若湿空气压缩过程按理想气体处理。试求压缩终了湿空气的相对湿度。
A.17.02kJ
B.-10.21kJ
C.-17.02kJ
D.10.21kJ
两个绝热容器各装有v(mol)的同种理想气体。最初两容器互相隔绝,但温度相同而压强分别为p1和p2,然后使两容器接通使气体最后达到平衡态。证明这一过程引起的整个系统熵的变化为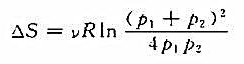 并证明△S>0。
并证明△S>0。
1 mol的单原子理想气体,其温度从T1=300 K升高到T2=350 K。求: (1)在容积不变的情况下,气体吸收的热量、增加的内能和对外做的功; (2)在压强不变的情况下,气体吸收的热量、增加的内能和对外做的功。
气体处理;30℃时水蒸气的饱和压力为42.45kPa。