 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某溶液中反应A+B→C.开始时反应物A与B的物质的量相.没有产物C.1h后A的转化率为75%,问2h后A尚有多少未反应?假设;(1)对A为一级反应,对B为零级反应;(2)对A,B皆为一级反应.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某溶液中反应A+B→C.开始时反应物A与B的物质的量相.没有…”相关的问题
更多“某溶液中反应A+B→C.开始时反应物A与B的物质的量相.没有…”相关的问题
A.滴定过程中消耗H+,使反应速率加快
B.滴定过程中产生H+,使反应速率加快
C.滴定过程中反应物浓度越来越小,使反应速率越来越快
D.反应产生Mn2+,它是KMnO4与H2O2反应的催化剂
E.反应产生O2,使反应速率加快
浓度和初始速率,见表3-2.

(1)写出反应速率方程
(2)计算25℃下反应速率系数;
(3)计算当c(C5H5N)=5.0x10-5mol·L-5,c(CH3l)=2.0x10-5mol·L-1时,相应的初始速率.
【题目描述】
第 3 题已知某两种物质在光照条件下能发生化学反应,观察其微观示意图(见下图),所得信息正确的是(说明:一种小球代表一种原子) ()。
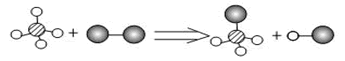 A.图示中共有4种分子
A.图示中共有4种分子
B.图示中的反应物没有单质
C.该反应属于置换反应
D.该图示不符合质量守恒定律
| 【我提交的答案】:B |
| 【参考答案与解析】: 正确答案:A |
答案分析:
【我的疑问】(如下,请求专家帮助解答)
反映物才3种那里来的4种。
某温度时,反应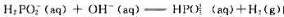 的反应速率与反应物浓度的关系如下表所示:
的反应速率与反应物浓度的关系如下表所示:

该反应的速率方程是()。
A、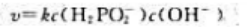
B、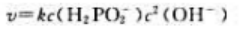
C、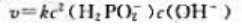
D、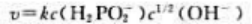
A.在酸度较高的溶液中,可形成MHY配合物
B.在碱性较高的溶液中,可形成MOHY配合物
C.不论形成MHY和MOHY,均有利于滴定反应
D.不论溶液中pH的大小,只形成MY一种配合物
E.反应物M和Y发生副反应不利于主反应的进行
根据下列问题的题意建立相应的微分方程,并列出初始条件(不具体解微分方程): (1)某化学反应的速率(反应物浓度x关于时间t的变化率)与反应物该瞬时的浓度x成正比(比例系数k>0),开始时的浓度为x0,求反应物浓度随时间变化的规律x(t); (2)已知曲线过点(1,2),其上任一点处的切线斜率为2x,求曲线方程y=F(x); (3)将一物体以初速度v0从地面竖直上抛(不计空气阻力),求物体上抛距离s关于时间t的变化规律s=s(t)(坐标原点设在地面).
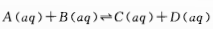 开始时只有A和B,经长时间反应,最终结果是()。
开始时只有A和B,经长时间反应,最终结果是()。A.C和D的浓度大于A和B的浓度
B. A和B的浓度大于C和D的浓度
C. A、B、C、D的浓度不再变化
D. A、B、C、D浓度相等
A.溶液的pH太高了
B.被滴定物浓度太小了
C.指示剂变色范围太宽了
D.反应产物的副反应严重了
E.反应物的副反应太少了