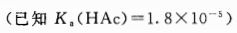题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
计算下列溶液的pH: 1、0.05 mol/L NaOAc 2、0.05 mol/L NH4Cl 3、0.1 mol/L NaCl 4、0.05 mol/L NaHCO3
暂无答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“计算下列溶液的pH: 1、0.05 mol/L NaOAc …”相关的问题
更多“计算下列溶液的pH: 1、0.05 mol/L NaOAc …”相关的问题
计算NaHA类型物质溶液的pH,常用的最简式为______,使用此最简式的条件是:(1)______(2)______。
用纯CaCO3标定EDTA溶液。称取0.1005g纯CaCO3,溶解后定容到100.00mL。吸取25.00mL,在pH=12.00时,用钙指示剂指示终点,用待标定的EDTA溶液滴定,用去24.50mL。试计算:
(1)EDTA溶液的物质的量浓度(2)该EDTA溶液对ZnO和Fe2O3的滴定度
①pH——-1的强酸溶液。加水稀释后,溶液中所有离子的浓度均降低;
②pH——-2的盐酸和pH=1的醋酸,c(H+)之比为2:1;
③在Na2C03和NaHC03溶液中均存在下列关系c(Na+)+c(H+)=c(OH一)+c(HC03-)+2c(c032-);

其归纳正确的是()。
A.①②③⑥
B.③④⑤⑥
C.②④⑤⑥
D.①③④⑤
0.35mol·L-1 HAc溶液与0.45mol·L-1NaAc 等体积混合,计算混合溶液的pH值。