 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
随后转化步骤是一个可逆的电极反应紧接着一个不可逆的化学反应,因此与电极可逆反应的极化曲线相比,其阴极极化曲线整体向负电势方向移动。()
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“随后转化步骤是一个可逆的电极反应紧接着一个不可逆的化学反应,…”相关的问题
更多“随后转化步骤是一个可逆的电极反应紧接着一个不可逆的化学反应,…”相关的问题
A.对不可逆极谱波,在起波处(即id
B.对不可逆极谱波,要使电活性物质在电极上反应,就必须有一定的活化能;
C.在不可逆极谱波的波中部,电流受电极反应和化学反应速度共同控制;
D.可逆与不可逆极谱波的半波电位之差,表示不可逆电极过程所需的过电位。
A.电极极化就是电极的电极电位偏离了由能斯特方程计算出来的平衡电位
B.原电池就是最原始的Cu-Zn电极组成的丹尼尔电池
C.电池的电动势为负值时就是原电池,否则就是电解池
D.可逆电极就是可以进行逆向电化学反应的电极
在pH4.75的乙酸盐缓冲溶液中,IO3-还原为I-的可逆极谱波的半波电位为+0.779 V(vs.SCE),试计算该电极反应的标准电极电位。
将反应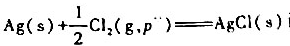 设计成原电池.已知25°C;时,
设计成原电池.已知25°C;时,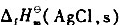 =-127.07kJ.mol-1.
=-127.07kJ.mol-1.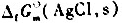 =-109.79kJ.mol-1,标准电极电势
=-109.79kJ.mol-1,标准电极电势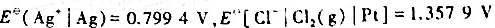 .
.
(1)写出电极反应和电池图示;
(2)求25°C、电池可逆放电2F电荷悬时的热Qz;
(3)求25°C时AgCl的活度积Kap.
二氯丙醇环化反应是合成甘油的一个中间步骤,主要反应为

当1,2-二氯丙醇和氢氧化钠的起始浓度均为0.328mol·L-1时,在温度31.2℃测得不同时间1,2-二氯丙醇的浓度为cA,其数值如下所示:
反应不同时间测得的cA值(单位:mol·L-1)
| 时间t/mln | 6.17 | 11.00 | 16.25 | 20.92 | 30.00 |
| cA c-1A | 0.175 5.70 | 0.124 8.06 | 0.093 10.70 | 0.078 12.80 | 0.059 17.00 |
试确定此反应的级数和转化速率常数K的数值。
A.滴定曲线是电流-滴定剂体积的关系图
B.滴定装置使用双铂电极系统
C.滴定过程存在可逆电对产生的电解电流的变化
D.要求滴定剂和被测物至少有一个为氧化还原电对
E.永停滴定法组成的是电解池
阅读下列材料,回答问题。
不久前的一个星期一,我照例批阅着学生的周记。突然,陆春的一篇作文《老师,我想对你说》闯入了我的眼帘。文中写道:“今天上午第三节课是数学课。铃声响过了好长时间,数学老师才晃着身子,穿着拖鞋,姗姗来迟。他大摇大摆地走进教室。也许是感冒或者其他原因,他干咳了几声,随后将一大口痰吐在了讲台旁,紧接着习惯性地把手往鼻子里抠了几下,并打开旁边饮水机的水龙头,将手洗了洗。如此行为既不雅观,也不文明,更不卫生,还让人觉得恶心……”
问题:请从教师职业道德的角度,评价材料中数学老师的行为。本案例对你有何启示?