 更多“实验中硬脂酸与氢氧化钠反应生成的产物是()。”相关的问题
更多“实验中硬脂酸与氢氧化钠反应生成的产物是()。”相关的问题
写出下列过程的反应方程式,并予以配平.
(1)金属镁在空气中燃烧生成两种二元化合物;
(2)在纯氧中加热氧化钡;
(3)氧化钙用来除去火力发电厂排出废气中的二氧化硫;
(4)唯一能生成氮化物的残金属与氮气反应;
(5)在消防队员的空气背包中,超氧化钾既是空气净化剂又是供氧剂;
(6)用硫酸锂同氢氧化钡反应制取氢氧化锟;
(7)镀是s区元索中唯一的两性元素,它与氢氧化钠水溶液反应生成了气体和澄清的溶液;
(8)铍的氢氧化物与氢氧化钠溶液混合;
(9)金属钙在空气中燃烧,将燃烧产物再与水反应.
阅读下列三段材料.根据要求完成任务。
材料一《普通高中化学课程标准(实验)》关于“几种重要的金属化合物”的内容标准是:根据生产、生活中的应用实例或通过实验探究,了解钠、铝、铁、铜等金属及其重要化合物的主要性质.能列举合金材料的重要应用。
材料二某版本高中实验教科书《化学1》“钠的重要化合物”的部分内容:
氧化钠和过氧化钠思考与交流
1.回忆前面做过的实验.描述氧化钠和过氧化钠的颜色、状态。
2.氧化钠与水的反应和氧化钙与水的反应类似,请你写出氧化钠与水反应的化学方程式。
实验3—5
把水滴入盛有少量过氧化钠固体的试管中,立即把带火星的木条放在试管口,检验生成的气体。用手轻轻摸一摸试管外壁,有什么感觉?然后向反应后的溶液中滴入酚酞溶液.有什么现象发生?
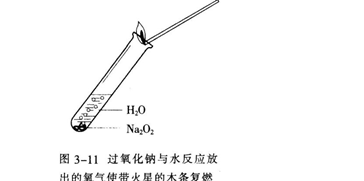
通过实验和观察.请你描述一下这些现象。过氧化钠与水反应生成氢氧化钠和氧气:2Na202+2H20=4NaOH+02↑
过氧化钠还能与二氧化碳反应生成碳酸钠和氧气:2Na202+2C02==2Na2C03+02↑
因此.过氧化钠可用于呼吸面具或潜水艇中氧气的来源。
材料三教学对象为高中一年级学生.他们已经学习了必须化学1的“从实验学化学…‘化学物质及其变化”和“金属的化学性质”等知识。
要求:
(1)回答材料二中“思考与交流”中的问题。
(2)完成“氧化钠和过氧化钠”的教学设计片段,内容包括教学目标、教学重难点和教学过程。并对教学过程做简要说明。(不少于300字)
阅读下面文字.回答有关问题:
人教版标准实验教科书中关于铜与浓硫酸反应的实验为:在一个带导管的胶塞侧面挖一个凹槽,并嵌入下端卷成螺旋状的铜丝。在试管里加入2mL浓硫酸.盖好胶塞,使铜丝与浓硫酸接触,加热。把放出的气体通入品红溶液或紫色石蕊溶液中,观察现象。向上拉铜丝,终止反应,冷却后,把试管里的液体慢慢倒入盛有少量水的另一支试管中.观察溶液的颜色。下面是某老师对此实验的改进:
如下图所示,配制浓度为5%的氢氧化钠溶液,并取适量的棉花蘸取,把蘸有氢氧化钠溶液的棉花塞在干燥管内,细管l:7也塞上。玻璃管上分别缠上品红试纸、蓝色石蕊试纸,浸有KMn0。溶液的布条。试管内加入2mL浓硫酸,按图连接装置。加热,待浓硫酸快要沸腾时撤离酒精灯.并把铜丝钩迅速放下,令反应的铜丝完全浸没在硫酸里,反应立即开始,可以看到白色烟雾的生成,待安全装置内的蓝色石蕊试纸变红,品红试纸和浸有KMn04。溶液的布条褪色时,将铜丝钩拉升,此时试管中溶液为蓝绿色,几乎没有黑色。反应完成后,静置5分钟,等多余的S02被棉花吸收为止。然后取下安全装置的试管,让同学体验S02的气味,加深印象。
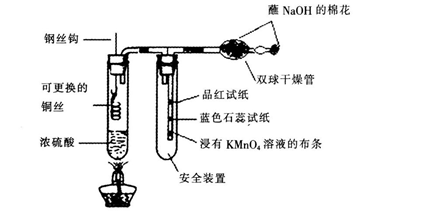
结合上述材料,简要回答问题:
(1)写出该改进实验设计的优点。(写出3个方面)
(2)简述上述改进实验操作的注意事项。
)用高锰酸钾的酸性水溶液氧化可得到一个酮(C)和一个羧酸(D)。而(B)与溴化氢作用得到的产物是(A)的异构体(E)。试写出(A)、(B)、(C)、(D)和(E)的构造式及各步反应式。
案例:
下面是某化学老师关于“乙醇”的课堂教学片段。
【导入】表演魔术——魔棒点灯。这无根之火怎么产生的?我们先从这种液体研究起。
【学生活动】通过观察液体的颜色、状态、气味,得出结论,并试着在学案上写出乙醇的物理性质。
【投影】乙醇的物理性质
【探究l】根据信息提示,推测乙醇可能的结构。
经实验测定,乙醇的分子式为C2H60,且分子中每个碳原子可连接四个原子、每个氧原子可
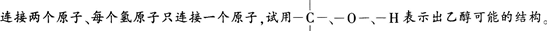
【学生活动】写出符合要求的可能结构。
【探究活动2】运用假设推理一实验验证一数据分析的方法确定乙醇的真实结构。【演示实验】乙醇与钠的反应并验证产物只有H:。
【思考与交流】由分子式C2H60推测,1 mol乙醇分子最多可提供——, mol氢原子参加反应,生成 ITIOl氢气分子。
【材料1】某化学兴趣小组关于“乙醇结构”的探究。
①量取2.9 mL的无水乙醇(约O.05 t001)于试管中,并加入足量的钠;②反应生成氢气体积标准状态为564 mL(约0.025 m01);
③通过讨论得出结论。【思考与交流】
①l tool乙醇实际生成了 mol氢气,mol氢原子。
②1个乙醇分子只能提供 个氢原子与Na反应生成氢气分子。
【追问】明明l个乙醇分子中含有6个氢原子,为什么却只能提供一个氢原子生成氢气呢?【学生活动】观察两种可能结构的球棍模型,根据这两种结构中氢所处位置的差异,确定乙醇的结构。
【师生互动】归纳乙醇的结构式、结构简式。
【对比】对比烧杯中钠与水、钠与乙醇的反应,根据钠与水反应的方程,尝试写出钠与乙醇的反应方程式。
乙醇与钠的反应实质:
CH3CH20H+Na→CH3CH20NaH2 ↑
【转引】从氧化还原的角度分析,乙醇在与钠的反应中做的是氧化剂,事实上,在大多数化学反应中.乙醇更愿意做还原剂。
【学生活动】根据有机反应方程式的书写规则,写出乙醇的燃烧方程式。
【探究3】材料一应用一实验探究乙醇的催化氧化反应。
【思考与交流】
①工厂高温焊接铜制器件时。表面生成黑的物质是什么?
②把发黑的铜制品趁热蘸一下酒精,就会恢复原有光泽,这又是什么原因。
【学生活动】根据桌上提供的仪器和药品,设计出合理的实验方案,通过实验,探究上述变化的可能原因。
【归纳总结】在铜或银作催化剂时,乙醇能被氧气氧化产生乙醛,我们称这个反应为乙醇的催化氧化反应。
问题:
(1)该教师在导入新课时,采用了哪种导入方法,并说明在教学实施过程中运用该导入法时应注意哪些问题。
(2)化学课堂上经常采用演示来完成教学,其构成要素及基本的类型有哪些?
(3)该教师在教学过程中,如何完成教学目标?
在600K时有反应2NO+O2→2NO2,NO和O2的初始浓度c(NO)和c(O2)及反应的初始速率υ的实验数据如下:
| c(NO)/(mol·L-1) | c(O2)/(mol·L-1) | υ/(mol·L-1·s-1) |
| 0.010 0.010 0.030 | 0.010 0.020 0.020 | 2.5×10-3 5.0×10-3 4.5×10-2 |
A.为苯氧乙酸类利尿药
B.与氢氧化钠煮沸后,其产物与变色酸、硫酸反应显蓝紫色
C.为中枢降压药
D.可使高锰酸钾溶液褪色
E.与水任意混溶


 如果结果不匹配,请
如果结果不匹配,请 

















