题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
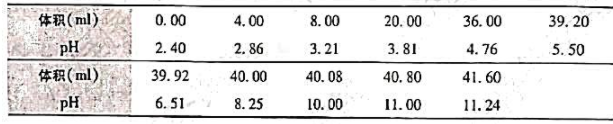
某一元弱酸(HA)纯晶1.250g,制成50ml水溶液。用NaOH溶液(0.0900moL)滴定至化学计量点,消耗41.20ml。在滴定过程中,当滴定剂加到8.24ml时,溶液的pH为4.30。计算①HA的摩尔质量;②HA的Ka</sub>;③化学计量点的pH。
某一元弱酸(HA)纯晶1.250g,制成50ml水溶液。用NaOH溶液(0.0900moL)滴定至化学计量点,消耗41.20ml。在滴定过程中,当滴定剂加到8.24ml时,溶液的pH为4.30。计算①HA的摩尔质量;②HA的Ka</sub>;③化学计量点的pH。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“某一元弱酸(HA)纯晶1.250g,制成50ml水溶液。用N…”相关的问题
更多“某一元弱酸(HA)纯晶1.250g,制成50ml水溶液。用N…”相关的问题
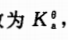 在水溶液中的解离度为α。若加等体积水稀释此洛液,则发生的变化是()。
在水溶液中的解离度为α。若加等体积水稀释此洛液,则发生的变化是()。
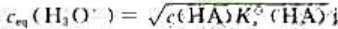 计算元弱酸HA溶液中,H3O+浓度,需要满足的两个条件是()和()。
计算元弱酸HA溶液中,H3O+浓度,需要满足的两个条件是()和()。