 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
标准状态下,由电对Ni2+/Ni和Pb2+/Pb组成电池。 (1)写出电池符号和电池反应方程式。 (2)计算电池电动势、电
标准状态下,由电对Ni2+/Ni和Pb2+/Pb组成电池。
(1)写出电池符号和电池反应方程式。
(2)计算电池电动势、电池反应的标准吉布斯自由能和平衡常数。
(3)在两电池溶液中同时加入S2-溶液,并使之都达到c(S2-)=1mol·L-1,求两电对的电极电势值,电池电动势和电池反应方向。
 答案
答案
(1)电池组成式为
(—)Ni|Ni2+(1 mol·L-1)||Pb2+(1 mol·L-1)|Pb(+)
电池反应:
Ni+Pb2+ Ni2++Pb
Ni2++Pb
(2) (Ni2+/Ni)=-0.257V,
(Ni2+/Ni)=-0.257V, (Pb2+/Pb)=-0.126V
(Pb2+/Pb)=-0.126V
E池=[-0.126-(-0.257)]V=0.131V
 =
= =-2×96500×0.131J·mol=25283J·mol
=-2×96500×0.131J·mol=25283J·mol
据 ,可得
,可得 =2.76×104。
=2.76×104。
(3)在两电极溶液中加入S2-,分别发生以下反应:
Ni2++S2- NiS↓, {c(Ni2+)}{c(S2-)}=Ksp(NiS)
NiS↓, {c(Ni2+)}{c(S2-)}=Ksp(NiS)
Pb2++S2- PbS↓, (c(Pb2+)}{c(S2-)}=Ksp(PbS)
PbS↓, (c(Pb2+)}{c(S2-)}=Ksp(PbS)
当c(S2-)=1 mol·L-1时
{c(Ni2+)}=Ksp(NiS), (c(Pb2+)}=Ksp(PbS)


此时 <0,故电池反应将逆向进行。
<0,故电池反应将逆向进行。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案

 更多“标准状态下,由电对Ni2+/Ni和Pb2+/Pb组成电池。 …”相关的问题
更多“标准状态下,由电对Ni2+/Ni和Pb2+/Pb组成电池。 …”相关的问题
 (Fe3+/Fe2+)=0.77V,
(Fe3+/Fe2+)=0.77V,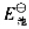 表示由上述两个电对组成的原电池的标准电动势,用K1和K2分别表示Co(OH)3和Co(OH)2的溶度积常数。试证明:
表示由上述两个电对组成的原电池的标准电动势,用K1和K2分别表示Co(OH)3和Co(OH)2的溶度积常数。试证明:

















