 更多“一定压力下,某物质液相转化为气相时的温度即为露点()”相关的问题
更多“一定压力下,某物质液相转化为气相时的温度即为露点()”相关的问题
和200.0g苯置于带活塞的导热容器中,始态为一定压力下90℃的液态混合物。在恒温90℃下逐渐降低压力,问:(1)压力降到多少时,开始产生气相,此气相的组成如何?(2)压力降到多少时,液相开始消失,最后一滴液相的组成如何?(3)压力为92.00kPa时,系统内气一液两相平衡,两相的组成如何?两相的物质的量各为多少?
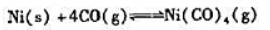
(1)不查附表,判断该反应是嫡增反应还是煽减反应.
(2)在某温度下该反应自发进行,推测反应自发进行时环境的璃是增加还是减少.
(3)利用附表一中所查到的数据,计算25℃下该反应的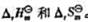
(4)当该反应的时,温度为多少?
(5)在提纯镍的Mond过程中,第一步是粗镍与CO,Ni(CO)4(四羰基合镍)在50℃左右的温度下达到平衡,这一步的标准平衡常数应尽可能的大,以便使镍充分地变成气相化合物.计算50℃下上述反应的标准平衡常数Kθ.
(6)在Mond过程中的第二步,将气体混合物从反应器中除去,并将其加热至230℃左右.在足够高的温度下的正、负号可以转换,反应在相反方向上发生,沉积出纯镍.在这一步,前述反应的标准平衡常数应尽可能的小.计算在230℃下该反应的标准平衡常数.
(7)Mond过程的成功依赖于Ni(CO)4的挥发性.在室温条件下,Ni(CO)4是液体,42.2℃时沸腾,其汽化焓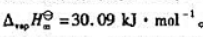 计算该化合物的汽化熵
计算该化合物的汽化熵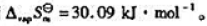
(8)近来改进了的Mond过程是在较高压力和150℃下进行第一步反应的.估算150℃下,Ni(CO)4,将要液化之前所能达到的最大压力(即估算150℃下,Ni(CO)4(l)的蒸气压).
在总压101.325kPa下,正庚烷—正辛烷的气液平衡数据如下。
 试求:(1)在总压101.325kPa下,溶液中正庚烷为0.35(摩尔分数)时的泡点及平衡气相的瞬间组成;(2)在总压101.325kPa下,组成x=0.35的溶液,加热到117℃,处于什么状态?(3)溶液加热到什么温度,全部气化为饱和蒸气?
试求:(1)在总压101.325kPa下,溶液中正庚烷为0.35(摩尔分数)时的泡点及平衡气相的瞬间组成;(2)在总压101.325kPa下,组成x=0.35的溶液,加热到117℃,处于什么状态?(3)溶液加热到什么温度,全部气化为饱和蒸气?
苯(1)一甲苯(2)可以作为理想系统。(1)求90℃时,与x1=0.3的液相成平衡的气相组成和泡点压力;(2)90℃和101.325kPa时的平衡汽、液相组成多少?(3)对于x1=0.55和y1=0.75的平衡系统的温度和压力各是多少?(4)y1=0.3的混合物气体在101.325kPa下被冷却到100℃时,混合物的冷凝率多少?
当混合物在一定的温度、压力下,满足( )条件即处于两相区,可通过( )计算求出其平衡汽液相组成。
气相反应2NO+2H2→N2+2H2O在某个温度下以等物质的量比的NO和H2混合气体在不同初压力下的半衰期如下表,试求反应总级数。
| p0/kPa | 50.0 | 45.4 | 38.4 | 32.4 | 26.9 |
| t1/2/min | 95 | 102 | 120 | 176 | 224 |


 如果结果不匹配,请
如果结果不匹配,请 

















