 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是()
A.用木炭还原氧化铜制取铜(加热):CuO+C ≜Cu+CO2 置换反应
B.服用含氢氧化铝的药物治疗酸过多症:2Al(OH)3+6HCl=2AlCl3+3H2O 复分解反应
C.煅烧石灰石制生石灰(高温):CaCO3 ≜CaO+CO2↑分解反应
D.用铁丝测定空气中氧气含量(点燃):3Fe+2O2 ≜Fe3O4化合反应
 答案
答案
BC
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.用木炭还原氧化铜制取铜(加热):CuO+C ≜Cu+CO2 置换反应
B.服用含氢氧化铝的药物治疗酸过多症:2Al(OH)3+6HCl=2AlCl3+3H2O 复分解反应
C.煅烧石灰石制生石灰(高温):CaCO3 ≜CaO+CO2↑分解反应
D.用铁丝测定空气中氧气含量(点燃):3Fe+2O2 ≜Fe3O4化合反应
 答案
答案
BC
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确…”相关的问题
更多“下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确…”相关的问题
A.用稀盐酸除铁锈 Fe2O3+6HCl=2FeCl2+3H2O
B.用二氧化碳制碳酸饮料 CO2+H2O=H2CO3
C.用电解水的方法测定水的组成 2H2O=2H2↑+O2↑
D.用氢氧化钠制碳酸钠 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
A.用赤铁矿高炉炼铁原理:Fe3O4+4CO 高温 3Fe+4CO2↑
B.正常雨水的pH约为5.6的原因:CO2+H2O=H2CO3
C.用氢氧化镁中和胃酸过多症:Mg(OH)2+H2SO4=MgSO4+2H2O
D.除去铜粉中少量的铁粉:2Fe+6HCl=2FeCl3+3H2↑
分子式为C3H7Br的有机物甲在适宜条件下能发生如图的一系列转化: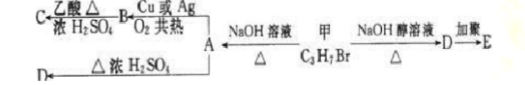 (1)若B能发生银镜反应,试回答下列问题:
(1)若B能发生银镜反应,试回答下列问题:
①试确定有机物甲的结构简式是();
②用化学方程式表示下列转化过程甲+NaOH溶液共热:()。B+Ag(NH3)OH:()。
(2)若B不能发生银镜反应试解答下列问题:
③试确定A的结构简式是();
④用化学方程式表示下列转化过程甲+NaOH的醇溶液共热:()。A→B:()。D→E:()。
A.定义:用化学式表示化学反应的式子叫化学方程式
B.意义:①表明了反应物、生成物和反应条件;②表明了反应物、生成物之间的质量关系,即各物质之间的质量比;③表明了反应物、生成物之间的微粒数关系
C.书写原则:遵循客观事实,依据质量守恒定律
利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下:其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+,Al3+,Ca2+,Mg2+。
(1)实验室用18.4mol·L的浓硫酸配制480mL4.6mol·L的硫酸,需量取浓硫酸()mL,配制时所用玻璃仪器除量筒、烧杯和玻璃棒外,还需()。
(2)酸浸时,为了提高浸取率可采取的措施有()。答出两点。
(3)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O72-,写出此反应的离子方程式()。
(4)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下: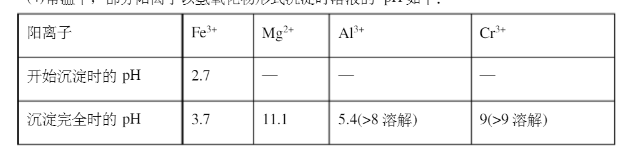 加入NaOH溶液使溶液呈碱性,既可以除去某些杂质离子,同时使Cr2O72-转化为CrO42-,但溶液的PH不能超过8,其理由是用离子方程式表示()。
加入NaOH溶液使溶液呈碱性,既可以除去某些杂质离子,同时使Cr2O72-转化为CrO42-,但溶液的PH不能超过8,其理由是用离子方程式表示()。
(5)钠离子交换树脂的反应原理为Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去滤液Ⅱ中的金属阳离子是()。
(6)写出上述流程中用SO2进行还原时发生反应的化学方程式:()。
下列化学方程式表示的反应,符合实验事实的是()。
A.Fe+CuSO4 Cu+FeSO4
B.2NaNO3+MgCl2 Mg(NO3)2+2NaCl
C.2Ag+2HCl2 AgCl↓+H2↑
D.2Fe+3H2SO4→ Fe2(SO4)3+3H2↑