 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在CuSO4溶液中加入下列物质①K②Na③Fe④Ag,能置换出铜单质的是()。
A.①
B.①②
C.③④
D.③
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.①
B.①②
C.③④
D.③
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在CuSO4溶液中加入下列物质①K②Na③Fe④Ag,能置换…”相关的问题
更多“在CuSO4溶液中加入下列物质①K②Na③Fe④Ag,能置换…”相关的问题
A.加入少量水,产生H2速率减小,H2体积减小
B.加入NH4HSO4固体,产生H2速率不变,H2体积不变
C.加入CH3COONa固体,产生H2速率减小,H2体积不变
D.滴加少量CuSO4溶液,产生H2速率变大,H2体积不变
某固体混合物中可能含有KI,SnCl2,CuSO4,ZnSO4,FeCl3,CoCl2和NiSO4。通过下列实验判断哪些物质肯定存在,哪些物质肯定不存在,并分析原因。
(1) 取少许固体溶入稀硫酸中,没有沉淀生成。
(2) 将盐的水溶液与过量氨水作用,有灰绿色沉淀生成,溶液为蓝色。
(3) 将盐的水溶液与KSCN作用,无明显变化。再加入戊醇,也无明显变化。
(4) 向盐的水溶液中加入过量NaOH溶液有沉淀生成,溶液无明显颜色。过滤后,向溶液缓慢滴加盐酸时,有白色沉淀生成。
(5) 向盐的溶液中滴加AgNO3溶液时,得到不溶于硝酸的白色沉淀。沉淀溶于氨水。
A.加入 NH4HSO4 固体
B.加入少量水
C.加入 CH3COONa 固体
D.滴加少量 CuSO4 溶液
A.Na2SO4、NaOH、Cu(OH)2
B.Na2SO4、CuCl2、HNO3
C.Na2SO4、NaOH、BaCl2
D.Na2CO3、CuSO4、H2SO4
解释实验现象。
(1)在煤气灯上加热KNO3晶体时没有棕色气体生成,但若KNO3晶体混有CuSO4时则有棕色气体生成。
(2)向KNO3的酸性溶液中加入Co(Ⅱ)盐,生成的K3[Co(NO2)6]沉淀中Co为+3价。
(3)向Na3PO4溶液中滴加AgNO3溶液时生成黄色沉淀,但向NaPO3溶液中滴加AgNO3溶液时却生成白色沉淀。
(4)向Na2HPO4溶液中加入CaCl2溶液有白色沉淀生成,但向NaH2PO4溶液中加入CaCl2溶液没有沉淀生成。
(5)分别向NaH2PO4,Na2HPO4和Na3PO4溶液中加入AgNO3溶液时,均得到黄色的Ag3PO4沉淀。
(6)向FeCl3溶液中滴加Na3PO4溶液,先有黄色沉淀生成;继续滴加时沉淀减少,最后消失得无色溶液。
(7)使AsH3通入一玻璃管,并在入口处加热,这时管壁出现有金属光泽的黑色物质。
(8)向含有Bi3+和Sn2+的澄清溶液中加入NaOH溶液会有黑色沉淀生成。
(9)将NaOH溶液与BiCl3溶液充分混合有白色沉淀生成,再向其中通入Cl2时有黄棕色沉淀生成。
A.在化合物中,碱金属元素的化合价均为+1
B.还原性:K>Na>Li,故K可从NaCl溶液中置换出金属Na
C.熔、沸点:Li>Na>K
D.碱性:LiOH<NaOH<KOH
根据标准电极电位数据,判断下列论述是否正确:
(1)在Cl-、Br-、I-溶液中,除I-外,其他离子都能被Fe3+氧化。已知: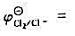

(2)用间接碘量法测定时CuSO4时,Fe3+能氧化I-析出I2,因而干扰CuSO4的测定,加入NH4HF2可消除此干扰。已知: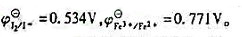
A.除去Fe粉中的SiO2可用强碱溶液
B.向一定量的AgNO3溶液中加入氨水至沉淀消失
C.向FeCl3溶液中加入KSCN溶液
D.向一定量的CuSO4溶液中加入氨水至沉淀消失
A.1 mol葡萄糖能水解生成2 mol CH3CH2OH和2 mol CO2
B.在鸡蛋清溶液中分别加入饱和Na2SO4溶液和 CuSO4 溶液,都会因盐析产生沉淀
C.油脂不是高分子化合物,1 mol油脂完全水解生成1 mol 甘油和3 mol高级脂肪酸(盐)
D.欲检验蔗糖水解产物是否具有还原性,可向水解后的溶液中直接加入新制的Cu(OH)2悬浊液并加热