 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
c(1/2H2SO4)=1mol·L-1与c(H2SO4)=0.5mol·L-1的溶液,其浓度完全相等。
c(1/2H2SO4)=1mol·L-1与c(H2SO4)=0.5mol·L-1的溶液,其浓度完全相等。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
c(1/2H2SO4)=1mol·L-1与c(H2SO4)=0.5mol·L-1的溶液,其浓度完全相等。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“c(1/2H2SO4)=1mol·L-1与c(H2SO4)=…”相关的问题
更多“c(1/2H2SO4)=1mol·L-1与c(H2SO4)=…”相关的问题
A.浓度完全相等
B.质量完全相等
C.物质的量相等
D.以上三者都对
A.KOH(aq)+1/2H2SO4(aq)===1/2K2SO4(aq)+H2O(l) ΔH=-11.46 kJ•mol-1
B.2KOH(aq)+H2SO4(aq)===K2SO4(aq)+2H2O(l) ΔH=-11.46 kJ·mol-1
C.2KOH(aq)+H2SO4(aq)===K2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
D.KOH(aq)+1/2H2SO4(aq)===1/2K2SO4(aq)+H2O(l) ΔH=-57.3 kJ•mol-1
A.c(Fe3+)<1mol·L-1
B.c(Fe2+)<1mol·L-1
C.c(Fe3+)/c(Fe2+)>1
D.c(Fe3+)/c(Fe2+)<1
Sn2+在1mol?L-1盐酸介质中还原而产生极谱波。25℃时,测得其平均极限扩散电流为4.25 IJLA,测得不同电位时的平均扩散电流值如下表所示:
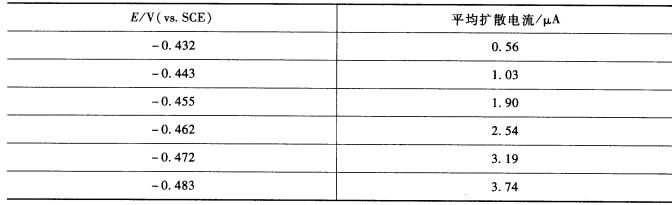 试求:(1)电极反应的电子数; (2)极谱波的半波电位; (3)电极反应的可逆性。
试求:(1)电极反应的电子数; (2)极谱波的半波电位; (3)电极反应的可逆性。
A.46 g 分子式为C2H6O 的有机物中含有的 C—H 键的数目为 6NA
B.1mol 甲烷完全燃烧转移的电子数为 8NA
C.1 L 0.1 mol•L-1 的乙酸溶液中含 H+的数量为 0.1NA
D.1 mol 的 CO 和 N2 混合气体中含有的质子数为 14NA
 (Fe3+/Fe2+)=0.77V,
(Fe3+/Fe2+)=0.77V, (Cu2+/Cu)=0.34V,则反应2Fe3+(1mol·L-1)+Cu====2Fe2+(1mol·L-1)+Cu2+(1mol·L-1)进行的方向是( )。
(Cu2+/Cu)=0.34V,则反应2Fe3+(1mol·L-1)+Cu====2Fe2+(1mol·L-1)+Cu2+(1mol·L-1)进行的方向是( )。A.呈平衡态
B.正向自发进行
C.逆向自发进行
D.无法判断
标准状态下,由电对Ni2+/Ni和Pb2+/Pb组成电池。
(1)写出电池符号和电池反应方程式。
(2)计算电池电动势、电池反应的标准吉布斯自由能和平衡常数。
(3)在两电池溶液中同时加入S2-溶液,并使之都达到c(S2-)=1mol·L-1,求两电对的电极电势值,电池电动势和电池反应方向。
A.增加
B.减少
C.不变
D.无法判断
A.1.01V
B.0.202V
C.0.889V
D.0.771V