 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
氢电极插入纯水,通H2(100kPa)至饱和,则其电极电势( )。
A.E=0
B.E>0
C.E<0
D.因未加酸不可能产生
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.E=0
B.E>0
C.E<0
D.因未加酸不可能产生
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“氢电极插入纯水,通H2(100kPa)至饱和,则其电极电势(…”相关的问题
更多“氢电极插入纯水,通H2(100kPa)至饱和,则其电极电势(…”相关的问题
有一个原电池由两个氢电极组成,其中有一个标准氢电极,为得到最大电动势,另一个电极浸入的酸性溶液[设p(H2)=100kPa]应为( )。
(A) 0.1mol·dm-3HCl (B) 0.1mol·dm-3HAc
(C) 0.1mol·dm-3H3PO4
(D) 0.1mol·dm-3HAc+0.1mol·dm-3NaAc
原电池的电池符号为: (-)Pt,H2(100kPa)丨H+(1.0molL-1) ‖ c12(100kPa)丨 Cl-(1.0molL-1)丨 Pt()
写出电极反应及电池反应;
298K时,有电池Pt|H2(100kPa)|HI(m)|AuI(S)|Au(s)。 (1)请写出各电极反应及电池反应。 (2)m=1×10-4mol/kg时,电动势E=0.97V;若m=3.0mol/kg时,E=0.41V。求m=3.0mol/kg时,HI的平均活度系数。 (3)已知Au+(aq)+e-→Au(8)的φΘ=1.68V,求AuI的溶度积。
用标准甘汞电极作正极,氢电极作负极(pH2=100kPa)与待测的HCl溶液组成电池。在25℃时,测得E=0.342V。当待测溶液为NaOH溶液时,测得E=1.050V。取此NaOH溶液20.00mL,用上述HCl溶液中和完全,需用HCl溶液多少毫升?
过度排放CO2会造成”温室效应“,科学家正在研究如何将CO2转化为可以利用的资源,其中一种方案就是将CO2转化为可再生燃料甲醇(CH3OH)。其化学方程式为: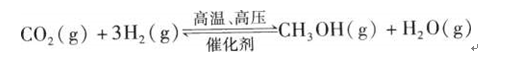
请填空:
问题一、写出上述反应的平衡常数表达式K=()。
问题二、在容积为2L的密闭容器中,用一定量二氧化碳与一定量氢气在一定条件下合成甲醇,实验结果如下图。以下说法正确的选项是()。
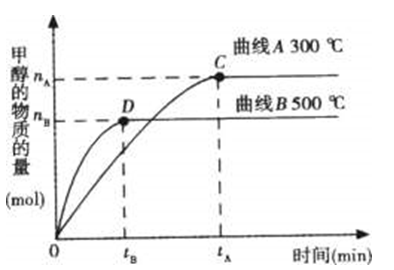
A在300℃,从反应开始到平衡,甲醇的平均反应速率
B反应体系从300℃升温到500℃,平衡常数K变大
C该反应的正反应为放热反应
D处于C点的反应体系从300℃升温到500℃n(H2)/n(CH3OH)增大
问题三、25℃、1.01×105Pa时16g液态甲醇完全燃烧,当恢复至原状态时,放出362.9kJ热量,此反应的热化学方程式为()。
问题四、选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此燃料电池负极应加入或通入的物质是,正极的电极反应式为()。
氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。
(1)可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。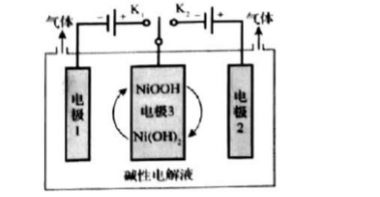 通过控制开关连接K1或K2,可交替得到H2和O2。
通过控制开关连接K1或K2,可交替得到H2和O2。
①制H2时,连接()。产生H2的电极反应式是()。
②改变开关连接方式,可得O2。
③结合①和②中电极3的电极反应式,说明电极3的作用()。
A.标准还原电势最大者
B.标准还原电势最小者
C.298K,P(H2)为任意值,aH,+=1时,氢电极的0=0
D.298K时氢电极的0=0
(1)爆炸反应后100C时H2的分压;
(2)反应前O2的体积;
(3)反应后85℃时气体的体积。
,测得E=1.050V,取此NaOH溶液20.00cm3,需上述HCl溶液多少立方厘米时才能完全中和? (已知25℃时,标准甘汞电极的电极电势为0.2828V,p(H2)=105Pa)