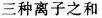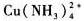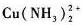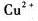题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知电极反应:Cu++e-=Cu的(Cu+/Cu)=0.52V,CuCl的=1.7X10-7。求电极反
已知电极反应:Cu++e-=Cu的(Cu+/Cu)=0.52V,CuCl的=1.7X10-7。求电极反
已知电极反应:Cu++e-=Cu的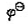 (Cu+/Cu)=0.52V,CuCl的
(Cu+/Cu)=0.52V,CuCl的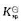 =1.7X10-7。求电极反应CuCl+e-=Cu+CI-的标准电极电势。
=1.7X10-7。求电极反应CuCl+e-=Cu+CI-的标准电极电势。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“已知电极反应:Cu++e-=Cu的(Cu+/Cu)=0.52…”相关的问题
更多“已知电极反应:Cu++e-=Cu的(Cu+/Cu)=0.52…”相关的问题
 (Cu2+/Cu)=0.337V,如果向此电极加入氨水,则电极电势( )。
(Cu2+/Cu)=0.337V,如果向此电极加入氨水,则电极电势( )。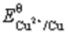 (Cu2+/Cu)=0.337V,
(Cu2+/Cu)=0.337V,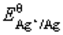 (Ag+/Ag)=0.80V。(提示:首先计算出反应平衡常数。)
(Ag+/Ag)=0.80V。(提示:首先计算出反应平衡常数。)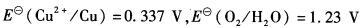 O2在Pt电极上的超电位为0.85 V,Cu的超电位为0 V)
O2在Pt电极上的超电位为0.85 V,Cu的超电位为0 V)