 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
含有0.02mol/L ZnY2+ 的pH=10的氨性缓冲溶液A、B两份,A溶液中含有0.3mo1/L的游离NH4B溶液中含有0.1mo1/L游离NH4.下列结论错误的是( )
A.A、B两溶液 不相等
不相等
B.A、B两溶液 不相等
不相等
C.A、B两溶液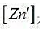 不相等
不相等
D.A、B两溶液[Zn2+]相等
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.A、B两溶液 不相等
不相等
B.A、B两溶液 不相等
不相等
C.A、B两溶液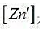 不相等
不相等
D.A、B两溶液[Zn2+]相等
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“含有0.02mol/L ZnY2+ 的pH=10的氨性缓冲溶…”相关的问题
更多“含有0.02mol/L ZnY2+ 的pH=10的氨性缓冲溶…”相关的问题
计算pH=5.0时Co2+和EDTA配合物的条件稳定常数(不考虑水解等副反应)。当Co2+抖浓度为0.02mol/L时,能否用EDTA准确滴定?
在Bi3+和Ni2+均为0.02mol/L时的混合溶液中,试求以EDTA溶液滴定时所允许的最小pH。能否采用控制溶液酸度的方法实现二者的分别滴定?
A.3%
B.6%
C.12%
D.30%
E.60%
称取制造油漆的填料红丹(Pb3O4)0.1000g,用盐酸溶解,在加热时加入0.02mol/L的K2Cr2O7溶液25mL,析出PbCrO4,反应为:2Pb2++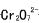 +H2O→2PbCrO4↓+2H+,冷却后过滤,将PbCrO4沉淀用盐酸溶解,加入KI和淀粉溶液,用0.1000mol/LNa2S2O3溶液滴定时,用去12.00mL。求试样中Pb3O4的质量分数。
+H2O→2PbCrO4↓+2H+,冷却后过滤,将PbCrO4沉淀用盐酸溶解,加入KI和淀粉溶液,用0.1000mol/LNa2S2O3溶液滴定时,用去12.00mL。求试样中Pb3O4的质量分数。
A.0.1~0.2g
B.0.16~0.32g
C.0.3~0.6g
D.0.6~0.8g
E.0.8~1.2g
用H型强酸性阳离子树脂去除海水中的Na+、K+(假设海水中仅存在这两种阳离子),已知树脂中H+的浓度为0.3mol/L,海水中Na+、K+的浓度分别为0.1mol/L和0.02mol/L,求交换平衡时溶液中Na+、K+的浓度。已知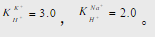
A.含有N、O、P、Q四个技术特征的电子锁
B.含有N、O两个技术特征的电子锁
C.含有N、O’、P三个技术特征的电子锁,其中O’是O的等同特征
D.含有N、O、Q三个技术特征的电子锁,其中Q不等同于P