 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
双光气分解反应CICOOCCl3(g)→2COCI2(g)为一级反应.将一定量双光气迅速引入一个280℃的容器中,751s后测得系统的压力为2.710kPa;经过很长时间反应完了后,系统压力为4.008kPa.在305℃时重复实验,经320s系统压力为2.838kPa;反应完了后系统压力为3.554kPa.求活化能.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“双光气分解反应CICOOCCl3(g)→2COCI2(g)为…”相关的问题
更多“双光气分解反应CICOOCCl3(g)→2COCI2(g)为…”相关的问题
体积为1dm3的抽空密闭容器中放有0.03458molN2O4(g),发生如下分解反应:

50℃时分解反应的平衡总压为130.0kPa.已知25℃时N2O4(g)和NO2(g)的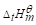
分别为9.16kJ·mol-1和33.18kJ·mol-1.设反应的ΔTGp,m=0.
(1)计算50℃时N2O4(g)的解离度及分解反应的Kθ;
(2)计算100C时反应的Kθ.
二氧化氮的分解反应2NO(g)→+2NO(g)+O2(g),319℃时,k1=0.498mol·L-1.
s-1;354℃时,k2=1.81mol·L-1.s-1.计算该反应的活化能E.和指前参最k0以及383℃时反应速率常数k.
℃下,每升气体会产生3.5×1029次·s-1的碰撞,如果每次碰撞都会发生化学反应,试计算HI的分解反应的速率.实验测定,该反应实际的反应速率是1.2×10-8·mol·dm-3·s-1,试求HI气体中活化分子的百分数(设每次活化分子的相互碰撞都产生反应).
A.0.0627
B.0.1026
C.0.1354
D.0.0513
在100℃下,于装有NH3(g)的密封容器中放入过量的NH4Cl(s),NH4Cl(s)发生分解反应:
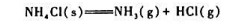
则系统的组分数C=(),相数P=(),自由度F=().
Fe3+可以作为H2O2歧化(分解)反应的催化剂.若该反应的机理为
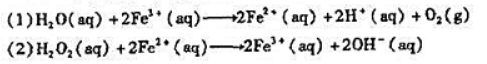
总反应:2H2O2(aq)→2H2O(l)+O2(g)
查出相关电对的标准电极电势,说明上述机理的可行性.并推断Ca2+催化H2O2分解的反应机理.
反应 ,开始阶段反应级数近似为3/2,在910K时速率常数为1.13 dm1.5·mol-0.5·S-1试计算C2H6(g)的压力为1.33X104Pa时的起始分解速率r[以c(C2H6)的变化表示]。
,开始阶段反应级数近似为3/2,在910K时速率常数为1.13 dm1.5·mol-0.5·S-1试计算C2H6(g)的压力为1.33X104Pa时的起始分解速率r[以c(C2H6)的变化表示]。
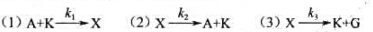 达稳态后,dex/dt=0,求:(1)反应速率-dcA/dt的-般表达式(式中不含X项);(2)k2》k3的反应速率简化表达式:(3)k3>>k2的反应速率简化表达式。
达稳态后,dex/dt=0,求:(1)反应速率-dcA/dt的-般表达式(式中不含X项);(2)k2》k3的反应速率简化表达式:(3)k3>>k2的反应速率简化表达式。
)和CO2(g)。当该分解反应达到平衡后,系统中共有压力不变的条件下将平衡系统中Na2CO3(s)除去·部分,化学平衡衡系统中的NaHCO3(s)全部除去,在其他条件不变时系统处于()。