 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在Fe3++e-=Fe2+电极反应中,加入F-,将使电极电势______;在Cu2++e-=Cu-电极反应中,加入Ⅰ-,将使电极电势______.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在Fe3++e-=Fe2+电极反应中,加入F-,将使电极电势…”相关的问题
更多“在Fe3++e-=Fe2+电极反应中,加入F-,将使电极电势…”相关的问题
A.c(Fe3+)<1
B.c(Fe2+)<1
C.c(Fe2+)/c(Fe3+)<1
D.c(Fe3+)/c(Fe2+)<1
A.(Fe3+/Fe2+)
B.(Fe3+/Fe2+)+
C.(Fe3+/Fe2+)+0.05916V
D.(Fe3+/Fe2+)-0.05916V
用K2Cr2O7标准滴定溶液在c(HCl)=1mol/L HCl溶液中滴定Fe2+,反应达化学计量点时的电位是1.02V,求此时Fe3+与Fe2+的浓度比。
 +6Fe2++14H+→2Cr3++6Fe3++7H2O中,达到化学计量点时,下列各种说法正确的是( )。
+6Fe2++14H+→2Cr3++6Fe3++7H2O中,达到化学计量点时,下列各种说法正确的是( )。A.溶液中c(Fe3+)与c(Cr3+)相等
B.溶液中不存在Fe2+和
C.溶液中两个电对Fe3+/Fe2+和
D.溶液中两个电对Fe3+/Fe2+和
已知在酸性溶液中,Fe2+与KMnO4反应时,1.00mL KMnO4溶液相当于0.1117gFe,而1.00mL KHC2O4·H2C2O4溶液在酸性介质中恰好与0.20mL上述KMnO4溶液完全反应。问需要多少毫升0.2000mol/L NaOH溶液才能与上述1.00mL KHC2O4·H2C2O4溶液完全中和?
计算298K时,Fe3+/Fe2+,c(Fe3+)=0.1mol·L-1, c(Fe2+)=0.5mol·L-1 电对的电极。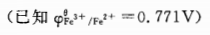
A.避免诱导反应的发生
B.加快反应的速率
C.使指示剂的变色点电位处在滴定体系的电位突跃范围内
D.终点易于观察
E.兼有C与D的作用
A.反应迅速进行
B.逆向进行
C.正向进行
D.不能确定
在适宜的条件下,所有可能发生的氧化还原反应中,条件电极电位值相差最小的电对之间首先进行反应。( )