 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
试判断下列各组中晶体的熔点,哪些高?哪些低?(1)CsCl,Au ,CO2,HCl; (2)NaCl,N2,NH3,Si(原子晶体);(3)Ca(OH)2,NaCl,N2;(4)N2,HF,BaCl2。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“试判断下列各组中晶体的熔点,哪些高?哪些低?(1)CsCl,…”相关的问题
更多“试判断下列各组中晶体的熔点,哪些高?哪些低?(1)CsCl,…”相关的问题
下列物质性质与应用的对应关系,正确的是()。
A.晶体硅熔点高、硬度大,可用于制作半导体材料
B.氢氧化铝具有弱碱性,可用于制胃酸中和剂
C.漂白粉在空气中不稳定,可用于漂白纸张
D.氧化铁能与酸反应.可用于制作红色涂料
试分别判断下列各组数据中哪个最大?哪个最小? (1)A=0.101B B=0.101D C=0.101H (2)A=1011B B=101 1D C=101 1H
A.G部:固定建筑物 F部:机械工程、照明
B.E部:电学 C部:化学、冶金
C.A部:人类生活必需 D部:纺织、造纸
D.H部:物理 B部:作业、运输
下列各组电子构型中哪些属于原子的基态?哪些属于原子的激发态?哪些纯属错误?
(1)ls22s1;
(2)ls22s22d1;
(3)1s13s1;
(4)ls22s22p43s1;
(5)1s32s22p4;
(6)ls22s22p63s23p6。
由共价键晶体组成的陶瓷材料,其性能特点不包括()
A.熔点高
B.硬度高
C.脆性小
D.强度高
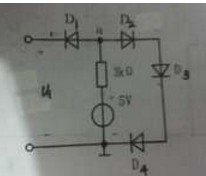
试判断图所示电路中,当Ui=3V时哪些二极管导通?当Ui=0V时哪些二极管导通?设二极管正向压降为0.7V。
下列各组离子中在强场八面体和弱场八面体中的晶体场稳定化能(CFSE)均相同的是.()。
(A)Ti 3+ 和 Cu 2+ ;
(B)Fe 2+ 和 Co 2+ ;
(C)Fe 3+ 和 Cr 3+ ;
(D)Co 3+ 和 Ni 2+ 。