 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
CO2分压为50kPa的混合气体,分别与CO2浓度为0.01kmol/m3的水溶液和CO2浓度为0.05kmol/m3。的水溶液接触。物系
CO2分压为50kPa的混合气体,分别与CO2浓度为0.01kmol/m3的水溶液和CO2浓度为0.05kmol/m3。的水溶液接触。物系温度均为2522,气液平衡关系P*=1.662×105kPa。试求:上述两种情况下两相的推动力(分别以气相分压力差和液相浓度差表示),并说明在CO:两种情况下属于吸收还是解吸。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“CO2分压为50kPa的混合气体,分别与CO2浓度为0.01…”相关的问题
更多“CO2分压为50kPa的混合气体,分别与CO2浓度为0.01…”相关的问题

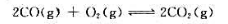
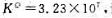 设在此温度下有由CO、O2和CO2组成的混合气体,它们的分压分别为1kPa、5kPa和100kPa,试计算此条件下反应的摩尔吉布斯自由能变。反应向哪个方向进行?如果CO和CO2的分压不变,要使反应向逆反应方向进行,O2的分压应是多少?
设在此温度下有由CO、O2和CO2组成的混合气体,它们的分压分别为1kPa、5kPa和100kPa,试计算此条件下反应的摩尔吉布斯自由能变。反应向哪个方向进行?如果CO和CO2的分压不变,要使反应向逆反应方向进行,O2的分压应是多少?
















