 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
两个含Zn2+的标准溶液浓度分别为25μg·mL-1、16μg·mL-1,在原子吸收光谱仪上测得它们的吸光度分别为0.480、0.35
两个含Zn2+的标准溶液浓度分别为25μg·mL-1、16μg·mL-1,在原子吸收光谱仪上测得它们的吸光度分别为0.480、0.350,在相同条件下测得试液的吸光度为0.422,求试液中Zn2+的浓度。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
两个含Zn2+的标准溶液浓度分别为25μg·mL-1、16μg·mL-1,在原子吸收光谱仪上测得它们的吸光度分别为0.480、0.350,在相同条件下测得试液的吸光度为0.422,求试液中Zn2+的浓度。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“两个含Zn2+的标准溶液浓度分别为25μg·mL-1、16μ…”相关的问题
更多“两个含Zn2+的标准溶液浓度分别为25μg·mL-1、16μ…”相关的问题
0.02mol·dm-3EDTA等浓度滴定Zn2+,在pH=10的NH4Cl-NH3缓冲溶液中,

0.02 mol·L-1EDTA等浓度滴定Zn2+,在pH=10.0的NH4Cl-NH3介质中若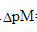 =0.2 mol·L-1,判断能否准确滴定。达化学计量点时,未络合的Zn2+百分数是多少?(pH=10.0时,αZn(OH)=102.4,lgαY(H)=0.5,lgKZnY=16.50,锌氨络合物的lgβ1~lgβ4分别为2.27、4.61、7.01、9.06
=0.2 mol·L-1,判断能否准确滴定。达化学计量点时,未络合的Zn2+百分数是多少?(pH=10.0时,αZn(OH)=102.4,lgαY(H)=0.5,lgKZnY=16.50,锌氨络合物的lgβ1~lgβ4分别为2.27、4.61、7.01、9.06
以2.0X10-2mol·L-1EDTA滴定浓度均为2.0X10-2mol·L-1的Al3+和Zn2+混合溶液中的Zn2+,在pH=5.5时,欲以KF掩蔽其中的Al3+,终点时游离KF的依度为1.0X10-8mol·L-1.计算说明在此条件下能否准确滴定Zn2+?已知:HF的pKθ=3.18;lgK(AIY)=16.1;lgKθ(ZnY)=16.5;pH=5.5时,
1ga[Y(H)]=5.5;AI3+-F-配合物的lgβ1θ~lgβ6θ分别为6.1,11.2,15.0,17.7,19.6,19.7.
在298K和标准压力下,用电解沉积法分离Cd2+、Zn2+混合溶液。已知Cd2+和Zn2+的浓度均为0.10 mol·kg-1(设活度因子均为1),H2(g)在Cd(s)和Zn(s)上的超电势分别为0.48 V和0.70V,设电解液的pH值保持为7.0。试问:(1)阴极上首先析出何种金属? (2)第二种金属析出时第一种析出的离子的残留浓度为多少?(3)氢气是否有可能析出而影响分离效果?