 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知化学反应式CH4(g)+CO2(g)===2CO(g)+2H2(g): (1)利用附录(在教材中)中各物质的,数据,求上述反应在25℃时
已知化学反应式CH4(g)+CO2(g)===2CO(g)+2H2(g):

(3)25℃时,若始态CH4(g)和CO2(g)的分压均为150kPa,末态CO(g)和H2(g)的分压均为50kPa,求反应的△rSm和△rGm。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知化学反应式CH4(g)+CO2(g)===2CO(g)+2H2(g):

(3)25℃时,若始态CH4(g)和CO2(g)的分压均为150kPa,末态CO(g)和H2(g)的分压均为50kPa,求反应的△rSm和△rGm。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知化学反应式CH4(g)+CO2(g)===2CO(g)+…”相关的问题
更多“已知化学反应式CH4(g)+CO2(g)===2CO(g)+…”相关的问题
A.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=+890.3kJ·molˉ1
B.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3kJ·molˉ1
C.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=+890.3kJ·molˉ1
D.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3kJ·molˉ1
已知CH3COOH(g),CH4(g)和CO2(g)的平均摩尔定压热容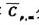 分别为52.3J·mol-1·K-1,37.7J·mol-1·K-1和31.4J·mol-1·K-1.试由教材附录中三化合物的标准摩尔生成焓计算1000K时下列反应的
分别为52.3J·mol-1·K-1,37.7J·mol-1·K-1和31.4J·mol-1·K-1.试由教材附录中三化合物的标准摩尔生成焓计算1000K时下列反应的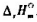 .
.
1
·K-1,37.7J·mol-1·K-1和31.4J·mol-1·K-1试由附录中三化合物的标准摩尔生成焓计算1000K时下列反应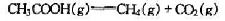 的
的
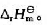
写出下列反应的平衡常数表达式(Kp,Kc和Kx都可以)。 (1)CH4(g)+2O2(g)=CO2(g)+2H2O(1) (2)2H2S(g)=2H2(g)+2S(s) (3)PbI2(s)=Pb2+(aq)+2I-(aq) (4)AgCl(s)+2NH3(aq)=Ag(NH3)2+(aq)+Cl-(aq)
0.05molCH4完全燃烧生成CO2气体和液态H2O时放出44.5kJ的热量。则下列热化学方程式中正确的是()。
A.2CH4(g)+4O2=2CO2(g)+4H2O(l)H=890kJ•mol-1
B.CH4+4O2=2CO2+4H2OH=890kJ•mol-1
C.CH4(g)+2O2=CO2(g)+2H2O(l)H=890kJ•mol-1
D.2CH4(g)+4O2=2CO2(g)+4H2O(l)H=890kJ•mol-1