 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某反应25℃时速率常数为1.3X10-3s-1,35℃时为3.6X10-1s-1.根据范特霍夫规则,估算该反应55℃时的速率常数.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某反应25℃时速率常数为1.3X10-3s-1,35℃时为3…”相关的问题
更多“某反应25℃时速率常数为1.3X10-3s-1,35℃时为3…”相关的问题
某化合物A的分解速率常数为0.29h-1,则此反应为______级反应,当c0=1.0mol·L-1时,此反应的半衰期为______,当c0=0.10mol·L-1时,此反应的半衰期为______。
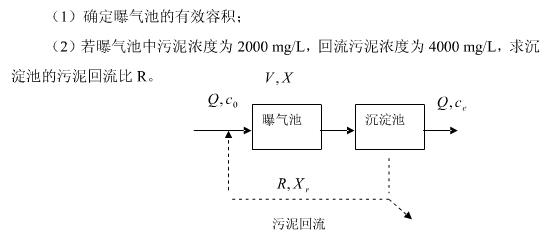
某城市生活污水采用完全混合曝气法处理,如图所示,水量为3×104m3/d,BOD5浓度为200mg/L,要求稳态运行时,出水BOD5浓度达到30mg/L,曝气池中有机物的降解遵循一级反应,反应速率常数为1.0d-1。
在不同温度下测得的某污染物催化分解反应的速率常数k如下表所示,求出反应的活化能和频率因子。
| 温度/K | 413.2 | 433.2 | 453.2 | 473.2 | 493.2 |
| k/(mol·g-1·h-1) | 2.0 | 4.8 | 6.9 | 13.8 | 25.8 |
A.正反应的活化能与逆反应的活化能相等
B.正反应的活化能大于逆反应的活化能
C.逆反应的活化能大于正反应的活化能
D.无法比较正、逆反应的活化能的相对大小
对于______反应,其反应级数一定等于反应物计量系数______,速率常数的单位由______决定,若k的单位为L2·mol-2·s-1,则对应的反应级数为______。
化合物A参加的一级反应速率常数k为0.082 0min-1,已知初始浓度c(A)0=0.150 0 molL-1,使c(A)t=0.030 0 molL-1需用多长时间___________;
微生物反应一般在常温附近进行时,其反应速率常数k与温度的关系可以用下式表示:
k=k20αt-20
式中:k20——20℃时的反应速率常数;
α——温度变化系数;
t——温度,℃。
试给出α与Arrhenius公式中活化能Ea的关系式。
一定温度下,对反应2A====B+D,实验测定了如下数据:
cA/(mol·L-1) 0.40 0.20
速率/(mol·L-1·min-1) 0.02 0.01
则该反应的速率方程为r=______,速率常数k=______。