 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在不同温度下测得的某污染物催化分解反应的速率常数k如下表所示,求出反应的活化能和频率因子。 温
在不同温度下测得的某污染物催化分解反应的速率常数k如下表所示,求出反应的活化能和频率因子。
| 温度/K | 413.2 | 433.2 | 453.2 | 473.2 | 493.2 |
| k/(mol·g-1·h-1) | 2.0 | 4.8 | 6.9 | 13.8 | 25.8 |
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在不同温度下测得的某污染物催化分解反应的速率常数k如下表所示,求出反应的活化能和频率因子。
| 温度/K | 413.2 | 433.2 | 453.2 | 473.2 | 493.2 |
| k/(mol·g-1·h-1) | 2.0 | 4.8 | 6.9 | 13.8 | 25.8 |
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在不同温度下测得的某污染物催化分解反应的速率常数k如下表所示…”相关的问题
更多“在不同温度下测得的某污染物催化分解反应的速率常数k如下表所示…”相关的问题
某温度下,N2O5按下式分解:
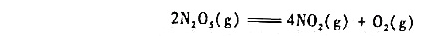
由实验测得在67℃时N2O5浓度随时间的变化如下:

试求:
(1)0-2min内的平均反应速率;
(2)t=2min时的瞬时反应速率。
某溶液的反应A+B→P,当A和B的起始浓度为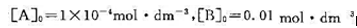 时,实验测得不同温度下吸光度随时间的变化如下表:
时,实验测得不同温度下吸光度随时间的变化如下表:
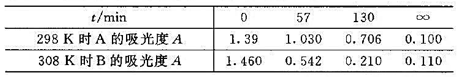
当固定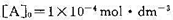 ,改变[B]o时,实验测得在298 K时,t1/2随[B]0的变化如下表:
,改变[B]o时,实验测得在298 K时,t1/2随[B]0的变化如下表:

设速率方程为r=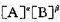 ,试计算α、β、速率常数k和实验活化能
,试计算α、β、速率常数k和实验活化能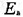 。
。
N2O(g)的热分解反应2N2O(g)====2N2(g)+O2(g),在一定温度下,反应的半衰期与起始压力成反比。在970K时,N2O(g)的起始压力为39.2kPa,测得半衰期为1529s;在1030K时,N2O(g)的起始压力为48.0kPa,测得半衰期为212s。求:

N2O5分解反应N2O5→2NO2+1/2O2是一级反应,已知其在某温度下的速率常数为4.8×10-4s-1。

碘在水中溶解度很小,但在含有l-的溶液中的溶解度增大,这是因为发生了反应:
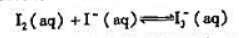
已经测得不同温度下的该反应的标准平衡常数结果见表4-1.

(1)画出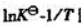 图;
图;
(2)估算该反应的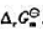 ;
;
(3)计算298K下该反应的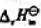 .
.
完成并配平下列化学反应方程式。
(1)高温下用氢气还原四氯化钛。
(2)在一定的温度和压强下以ZnO-Cr2O3催化一氧化碳与氢气的反应。
(3)在乙醚中氢化锂与三氯化铝反应。
(4)高温下二氧化碳与氢化钡作用。
(5)二氟化氙在水中缓慢水解。
(6)向三氧化氙的碱性溶液中通入臭氧。
(7)六氟化氙与二氧化硅反应。
(8)四氟化氙在水中歧化分解。
(9)六氟化氙的完全水解。
(10)六氟化氙的不完全水解。
(11)浓硫酸使高氙酸盐脱水。