 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
已知450℃时,反应H2(g)+I2(g)2HI(g)的K=100,由此推测在450℃时,反应1/2H2(g)+1/2I2(g)HI(g)的化学平衡常数为()
A.50
B.0.01
C.10
D.无法确定
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.50
B.0.01
C.10
D.无法确定
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知450℃时,反应H2(g)+I2(g)2HI(g)的K=…”相关的问题
更多“已知450℃时,反应H2(g)+I2(g)2HI(g)的K=…”相关的问题
氯气和碘蒸气反应用下列反应式表示;.
H2(g)+I2(g)=2HI(g)
在713.15K,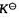 =50.0。如用下列反应式表示时:
=50.0。如用下列反应式表示时:

计算713.15K时它们的平衡常数 。
A.239.2kJ
B.438.4kJ
C.119.6kJ
D.358.8kJ
已知生产水煤气反应:
C(s)+H2O(g)=CO(g)+H2(g)
在1000K时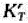 =1.00,若于密闭反应罐中通入1×105Pa的水汽与足量的红热碳反应,试确定平衡时诸气体的压力和水汽的转化率.
=1.00,若于密闭反应罐中通入1×105Pa的水汽与足量的红热碳反应,试确定平衡时诸气体的压力和水汽的转化率.
时水的饱和蒸气压为3.1663kPa,水的密度为997kg/m3。求298.15K反应H2(g)+1/2O2(g)=H2O(l)的ΔrGƟm。
A.K1+K2+K3
B.K1-K2-K3
C.K1K2K3
D.K1K3/K2
一定条件下,Ag与H2S可能发生下列反应: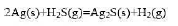 25°C,100kPa下,将Ag置于体积比为10:1的H2(g)与H2S(g)混合气体中。
25°C,100kPa下,将Ag置于体积比为10:1的H2(g)与H2S(g)混合气体中。
(1)Ag是否会发生腐蚀而生成Ag2S?
(2)混合气体中H2S气体的体积分数为多少时,Ag不会腐蚀生成Ag2S?
已知25°C时,H2S(g)和Ag2S(s)的标准生成吉布斯函数分别为-33.56kJ·mol-1和-40.26kJ·mol-1.
已知NO与H2可进行如下化学反应:
2NO(g)+2H2(g)→N2(g)+2H2O(g)
在一定温度下,某密闭容器中等摩尔比的NO与H2混合物在不同初始压力下的半衰期如下:

求反应的总级数n.