 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
一理想电池正在工作,在电池内部,已知将2C正电荷从“+”极移到“-”极,库仑电场力作功6J,试给出电池的电动势E值,
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“一理想电池正在工作,在电池内部,已知将2C正电荷从“+”极移…”相关的问题
更多“一理想电池正在工作,在电池内部,已知将2C正电荷从“+”极移…”相关的问题
A.挤压电池,直到不再鼓胀为止
B.将电池留在工作台上,并让所有人离开房间 15 分钟
C.使用工具戳刺鼓胀的电池
D.电池破裂,然后清理碎屑
准确量取30.00 mL弱酸HA,加水稀释至100.00 mL,在电池:(—)SHE|HA || SCE()中,以0.100 0 mol·L-1NaOH标准溶液滴定之。25℃时,当弱酸HA被中和一半时,电池电动势为0.524 V,化学计量点时,电池电动势为0.749 V。求:(1)弱酸HA的电离常数Kα值。(2)原弱酸HA溶液的浓度?(已知饱和甘汞电极的电极电位为0.244 V)
将反应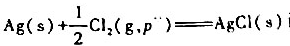 设计成原电池.已知25°C;时,
设计成原电池.已知25°C;时,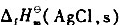 =-127.07kJ.mol-1.
=-127.07kJ.mol-1.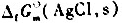 =-109.79kJ.mol-1,标准电极电势
=-109.79kJ.mol-1,标准电极电势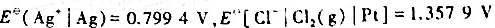 .
.
(1)写出电极反应和电池图示;
(2)求25°C、电池可逆放电2F电荷悬时的热Qz;
(3)求25°C时AgCl的活度积Kap.
已知PbSO4+2e-===Pb+SO42- Eθ===一0.359 V,Pb2++2e-===Pb Eθ=一0.126 V,当c(Pb2+)=0.100 mol.L-1,c(SO42-)=1.00 mol.L-1时,由PbSO4/Pb和Pb2+/Pb两个半电池组成原电池: (1)写出该原电池的符号及电池反应方程式; (2)计算该原电池的电动势E; (3)计算PbSO4的溶度积Kspθ。
A.1 将车辆停靠在路边;2按下灭火装置开关 3关闭钥匙和电源总开关
B.4及时组织车上人员有序撤离;5通知相关负责人; 6如火势不能控制,拨打119
19,有电池Pt|H2(




 H+(
H+(

