 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
试计算0.1mol·dm-3的H2SO4溶液中,各物种的浓度及溶液的pH值(H2SO4的Ka=1.2×10-2).
试计算0.1mol·dm-3的H2SO4溶液中,各物种的浓度及溶液的pH值(H2SO4的Ka=1.2×10-2).
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“试计算0.1mol·dm-3的H2SO4溶液中,各物种的浓度…”相关的问题
更多“试计算0.1mol·dm-3的H2SO4溶液中,各物种的浓度…”相关的问题
计算0.010mol·dm-3的H2SO4溶液中各离子的浓度,已知H2SO4的Kθ2为1.2×10-2。
写出以下电池的电极反应、电池反应方程式,并计算电池电动热.
(1)Zn|Zn2+(1×10-6mol·dm-3)||Cu2+(0.01mol·dm-3)|Cu
(2)Cu|Cu2+(0.01mol·dm-3)||Cu2+(2.0mol·dm-3)|Cu
(3)Pt,H2(1×105Pa)|HAc(0.1mol·dm-3)KCl(饱和),Hg2Cl2|Hg
将1.00mol·dm-3HAc溶液和1.00mol·dm-3氢氟酸等体积混合,若已知HAc的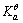 =1.8×10-5,HF的
=1.8×10-5,HF的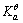 =6.3×10-4,试计算此溶液的c(H+),c(Ac-)和c(F-)。
=6.3×10-4,试计算此溶液的c(H+),c(Ac-)和c(F-)。
A.25:1
B.1:25
C.40:1
D.1:40
对于乙醇介质中发生的反应:
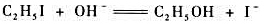
测得其288.83K时的速率常数k=5.03×10-5mol-1·dm-3·s-1,305.02K时的速率常数k=3.68×10-4mol-1·dm-3·s-1。试求该反应的活化能,并计算363.6IK时的速率常数。
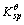 =1.2×10-10,SrCrO4的
=1.2×10-10,SrCrO4的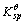 =2.2×10-5。
=2.2×10-5。
℃下,每升气体会产生3.5×1029次·s-1的碰撞,如果每次碰撞都会发生化学反应,试计算HI的分解反应的速率.实验测定,该反应实际的反应速率是1.2×10-8·mol·dm-3·s-1,试求HI气体中活化分子的百分数(设每次活化分子的相互碰撞都产生反应).