 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在1mol·L-1HC1溶液中用Fe3+溶液滴定Sn2+时,计算:(1)此氧化还原反应的平衡常数及化学计量点时反应进行的程度:滴定时电位突跃范围.在此滴定中应选用什么指示剂?用所选指示剂时,滴定终点是否和化学计量点一致?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在1mol·L-1HC1溶液中用Fe3+溶液滴定Sn2+时,…”相关的问题
更多“在1mol·L-1HC1溶液中用Fe3+溶液滴定Sn2+时,…”相关的问题
用K2Cr2O7标准滴定溶液在c(HCl)=1mol/L HCl溶液中滴定Fe2+,反应达化学计量点时的电位是1.02V,求此时Fe3+与Fe2+的浓度比。
在1mol/L HCl溶液中,用Fe3+滴定Sn2-,计算下列滴定百分数时的电位:9%、50%、91%、99%、99.9%、100%、100.1%、101%、110%、200%。
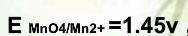 ,
,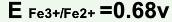 ,在此条件下用KMnO4标准溶液滴定Fe2+,其化学计量点时电位值是( )。
,在此条件下用KMnO4标准溶液滴定Fe2+,其化学计量点时电位值是( )。A.0.77V
B.1.06V
C.1.32V
D.1.45V
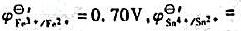 0.14V)
0.14V)
下表加入不同量的10μg·mL-1Fe2+标准溶液,再加1.0mL 100g·L-1盐酸羟胺溶液(用以将试液中Fe3+还原为Fe2+),2.0mL 1.5g·L-1邻二氮菲(与铁形成橘红色配合物)和5.0mL 1mol·L-1NaAc溶液(为减少其他离子干扰,以控制pH≈5的溶液中显色)再用水稀释至刻度,在510nm处测定吸光度,试计算试液中Fe的浓度?
| 编 号 | 空白 | 1 | 2 | 3 | 4 | 5 |
| 未知试液/mL | 0.0 | 10.0 | 10.0 | 10.0 | 10.0 | 10.0 |
| 10μg·mL-1Fe2+标准溶液/mL | 0.0 | 0.0 | 10.0 | 15.0 | 20.0 | 25.0 |
| 吸光度A | 0.040 | 0.201 | 0.291 | 0.341 | 0.381 | 0.432 |
·L-1HC1溶液后,溶液的pH有何变化?
(2)若在100mL pH=5. 00的HAe-NaAc级冲溶液中加入1.0mL,6.0mol·L-1NaOH后,溶液的pH增大0.10单位。问此级缓冲溶液中HAc、NaAc的分析浓度各为多少?
已知在1mol/L HCl介质中,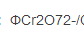 /Cr3+)=1.00V,
/Cr3+)=1.00V,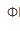 (Fe3+/Fe2+)=0.68V,以K7Cr2O7滴定Fe2+时,适宜的指示剂为( )。
(Fe3+/Fe2+)=0.68V,以K7Cr2O7滴定Fe2+时,适宜的指示剂为( )。
A.自身作指示剂 B.邻苯氨基苯甲酸(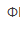 =0.89V)
=0.89V)
C.亚甲基蓝(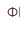 =0.52V)D.邻二氮菲亚铁(
=0.52V)D.邻二氮菲亚铁(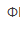 =1.06V)
=1.06V)
 (Fe3+/Fe2+)=0.77V,
(Fe3+/Fe2+)=0.77V, (Cu2+/Cu)=0.34V,则反应2Fe3+(1mol·L-1)+Cu====2Fe2+(1mol·L-1)+Cu2+(1mol·L-1)进行的方向是( )。
(Cu2+/Cu)=0.34V,则反应2Fe3+(1mol·L-1)+Cu====2Fe2+(1mol·L-1)+Cu2+(1mol·L-1)进行的方向是( )。A.呈平衡态
B.正向自发进行
C.逆向自发进行
D.无法判断
A.增加
B.减少
C.不变
D.无法判断