 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
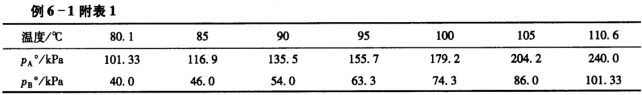
已知甲苯、苯在90℃下纯液体的饱和蒸气压分别为54.22kPa和136.12kPa。两者可形成理想液态混合物。取200.0g甲苯
和200.0g苯置于带活塞的导热容器中,始态为一定压力下90℃的液态混合物。在恒温90℃下逐渐降低压力,问:(1)压力降到多少时,开始产生气相,此气相的组成如何?(2)压力降到多少时,液相开始消失,最后一滴液相的组成如何?(3)压力为92.00kPa时,系统内气一液两相平衡,两相的组成如何?两相的物质的量各为多少?
 答案
答案




 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案

 更多“已知甲苯、苯在90℃下纯液体的饱和蒸气压分别为54.22kP…”相关的问题
更多“已知甲苯、苯在90℃下纯液体的饱和蒸气压分别为54.22kP…”相关的问题
 =23.06kPa,
=23.06kPa, =10.05kPa。假设低压下汽液平衡,确定给定的状态:
=10.05kPa。假设低压下汽液平衡,确定给定的状态:

 ,试求该温度下当液相组成x1=0.2时的汽相组成和压力。
,试求该温度下当液相组成x1=0.2时的汽相组成和压力。
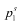 =1.343atm,
=1.343atm,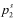 =0.535atm,则汽液平衡组成x1和y1分别是( )。
=0.535atm,则汽液平衡组成x1和y1分别是( )。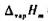 =40.668kJ·mol-1.求在100℃,101.325kPa下使1kg水蒸气全部凝结成液体水时的Q,W,ΔU和ΔH.设水蒸气适用理想气体状态方程.
=40.668kJ·mol-1.求在100℃,101.325kPa下使1kg水蒸气全部凝结成液体水时的Q,W,ΔU和ΔH.设水蒸气适用理想气体状态方程.
















