 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在锌电极上析出氢气的Tafel公式为 η/V=0.72+0.116lg[j/(A·cm-2)] 在298K时,用Zn(s)作阴极,惰性物质作阳极
在锌电极上析出氢气的Tafel公式为
η/V=0.72+0.116lg[j/(A·cm-2)]
在298K时,用Zn(s)作阴极,惰性物质作阳极,电解浓度为0.1mol·kg-1的ZnSO4溶液,设溶液pH值为7.0,若要使H2(g)不和锌同时析出,应控制什么条件?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在锌电极上析出氢气的Tafel公式为
η/V=0.72+0.116lg[j/(A·cm-2)]
在298K时,用Zn(s)作阴极,惰性物质作阳极,电解浓度为0.1mol·kg-1的ZnSO4溶液,设溶液pH值为7.0,若要使H2(g)不和锌同时析出,应控制什么条件?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在锌电极上析出氢气的Tafel公式为 η/V=0.72+0.…”相关的问题
更多“在锌电极上析出氢气的Tafel公式为 η/V=0.72+0.…”相关的问题
在含有1.000 mol?L-1硫酸锌与1.000 mol?L-1硫酸镉的1.0 mol?L-1的硫酸介质中,进行电解实验。
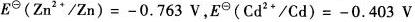 试计算:(1)电解时,锌和镉何者先析出? (2)能否在实验中完全分离锌和镉? (3)在铂和汞电极上,氢的析出是否干扰锌和镉的析出?(已知在铂和汞电极上的ηH2分别为一0.2 V和一1.0 V,ηZn和ηcd均为零)。
试计算:(1)电解时,锌和镉何者先析出? (2)能否在实验中完全分离锌和镉? (3)在铂和汞电极上,氢的析出是否干扰锌和镉的析出?(已知在铂和汞电极上的ηH2分别为一0.2 V和一1.0 V,ηZn和ηcd均为零)。
298K时,以Pt为阳极,Fe为阴极,电解浓度为1mol·kg-1的NaCl水溶液(活度因子为0.66)。设电极表面有H2(g)不断逸出时的电流密度为0.1 A·cm-2 ,Pt逸出CI2(g)的超电势可近似视为零。若Tafel公式为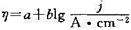 ,且Tafel常数a=0.73 V,b= 0.11 v,
,且Tafel常数a=0.73 V,b= 0.11 v,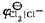 =1. 36 V,请计算实际的分解电压。
=1. 36 V,请计算实际的分解电压。
用镀铜的铂网电极作阴极,电解1.000×10-2mol·L-1zn2+溶液,试计算金属锌析出的最低pH。(已知
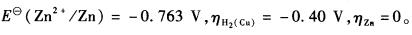
解释以下事实:
(1)单质铁与盐酸作用的产物是FeCl2,但在与氯气反应时的产物是FeCl3.
(2)单质银没有氢活泼,但Ag可从Hl溶液中置换出氢气.
(3)硝酸钠或稀硫酸溶液都没有明显的氧化性,例如,它们都不可能氧化Fe2+为Fe3+,但二者结合后都可以使Fe2+氧化为Fe3+.
(4)久置于空气的H2S溶液会变浑浊.
(5)Fel3,Cul2等化合物不存在.
(6)在碱性溶液条件下,金属铁可得到暂时性保护.
(7)用简单的锌盐及铜盐混合液进行电镀时,锌和铜不会同时析出.但在混合离子溶液中加入NaCN溶液,可使Cu,Zn同时析出.
A.碱性溶液能使酚酞试液变红,滴入酚酞试液后变红的溶液一定呈碱性
B.锌和铜均是金属,锌与稀硫酸反应生成氢气,则铜也能与稀硫酸反应生成氢气
C.酸能使石蕊试液变红,CO2也能使紫色的石蕊试液变红,所以CO2是酸
D.溶液中有晶体析出,其溶质质量减小,所以溶质的质量分数一定减小
在298K和标准压力下,用电解沉积法分离Cd2+、Zn2+混合溶液。已知Cd2+和Zn2+的浓度均为0.10 mol·kg-1(设活度因子均为1),H2(g)在Cd(s)和Zn(s)上的超电势分别为0.48 V和0.70V,设电解液的pH值保持为7.0。试问:(1)阴极上首先析出何种金属? (2)第二种金属析出时第一种析出的离子的残留浓度为多少?(3)氢气是否有可能析出而影响分离效果?
某试液含有1.000 m?L -1 Cu2+和1.000×10-2mol?L-1Ag+,若以铂电极进行电解,在阴极上首先析出的是铜还是银?两种离子是否可以电解分离?(
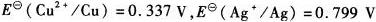 )
)