题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在298K和标准压力下,用电解沉积法分离Cd2+、Zn2+混合溶液。已知Cd2+和Zn2+的浓度均为0.10 mol
在298K和标准压力下,用电解沉积法分离Cd2+、Zn2+混合溶液。已知Cd2+和Zn2+的浓度均为0.10 mol·kg-1(设活度因子均为1),H2(g)在Cd(s)和Zn(s)上的超电势分别为0.48 V和0.70V,设电解液的pH值保持为7.0。试问:(1)阴极上首先析出何种金属? (2)第二种金属析出时第一种析出的离子的残留浓度为多少?(3)氢气是否有可能析出而影响分离效果?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“在298K和标准压力下,用电解沉积法分离Cd2+、Zn2+混…”相关的问题
更多“在298K和标准压力下,用电解沉积法分离Cd2+、Zn2+混…”相关的问题
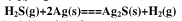

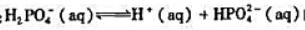 的标准平衡常数.
的标准平衡常数.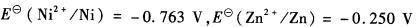 )
)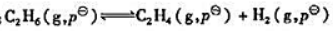 的
的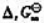 并判断在标准状态下反应向何方进行.
并判断在标准状态下反应向何方进行.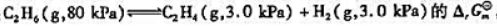 并判断反应方向.
并判断反应方向.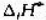 =-30.6kJ·mol-1,
=-30.6kJ·mol-1,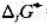 =-11.2kJ·mol-1,试求在298K时
=-11.2kJ·mol-1,试求在298K时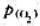 的压力是多少(Pa)?Ag2O(s)的热分解温度是多少?(105Pa下)
的压力是多少(Pa)?Ag2O(s)的热分解温度是多少?(105Pa下)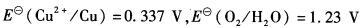 O2在Pt电极上的超电位为0.85 V,Cu的超电位为0 V)
O2在Pt电极上的超电位为0.85 V,Cu的超电位为0 V)