 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
<4> 、观察人体对于新药的耐受程度和药代动力学的是()
A.I 期临床试验
B.Ⅱ 期临床试验
C.Ⅲ 期临床试验
D.Ⅳ 期临床试验
 答案
答案
A、I 期临床试验
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.I 期临床试验
B.Ⅱ 期临床试验
C.Ⅲ 期临床试验
D.Ⅳ 期临床试验
 答案
答案
A、I 期临床试验
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“ 、观察人体对于新药的耐受程度和药代动力学的是()”相关的问题
更多“ 、观察人体对于新药的耐受程度和药代动力学的是()”相关的问题
观察人体对于新药的耐受程度和药代动力学的是()
A.I期I临床试验
B.Ⅱ期临床试验
C.Ⅲ期临床试验
D.Ⅳ期临床试验
E.生物等效性试验 根据《药品注册管理办法》:
A.0期临床试验
B.新药Ⅰ期临床试验
C.新药Ⅱ期临床试验
D.生物等效性试验
A.Ⅰ期临床试验
B.Ⅱ期临床试验
C.Ⅲ期临床试验
D.Ⅳ期临床试验
E.0期临床试验
A.观察人体对于新药的耐受程度和药代动力学,为制定给药方案提供依据
B.初步评价药物对目标适应症患者的治疗作用和安全性
C.其目的是进一步验证药物对目标适应证患者的治疗作用和安全性,评价利益与风险关系,最终为药物注册申请的审查提供充分的依据
D.考察在广泛使用条件下的药物的疗效和不良反应、评价在普通或者特殊人群中使用的利益与风险关系以及改进给药剂量等
B、临床方案设计
C、临床前研究:临床前药理学、毒理学、动物体内药效动力学及药代动力学
D、在人体内的作用:人体药代动力学、安全性及疗效以及市场应用经验,如注明已上市的国家以及所有上市后累积经验的重要资料(如处方、剂量、用法和不良反应等)
E、资料概要及研究者指南,即向研究者提供对新药可能出现的危险、药物过量和不良反应以及临床试验中可能需要的特殊检查、观察和预防措施的正确解释
表1 两组患者用药后有效率比较
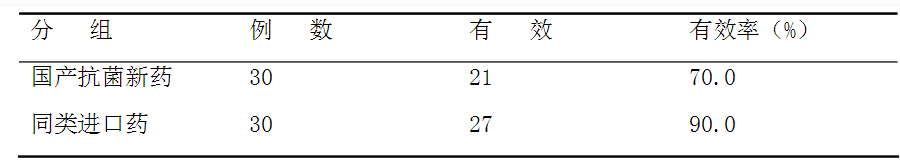
【问题】
(1)该研究属何种类型?
(2)在设计的过程中是否遵循了实验设计的基本原则?
(3)该临床试验为何种对照?
(4)该医师的结论是否可靠?为什么?
A.无发作时间不足12个月(服药前发作间期<4个月)
B.有效治疗剂量使用6个月以上
C.治疗剂量未达到50%DDD
D.因为不能耐受不良反应而在未达到观察期或治疗剂量前被迫停药
E.不到3个治疗前发作间期