 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在H3PO4存在下的HCl溶液中,用0.1mol/LK2Cr2O7溶液滴定0.1mol/L Fe2+溶液时,已知化学计量点的电位为0.86V。最
在H3PO4存在下的HCl溶液中,用0.1mol/LK2Cr2O7溶液滴定0.1mol/L Fe2+溶液时,已知化学计量点的电位为0.86V。最合适的指示剂为( )。
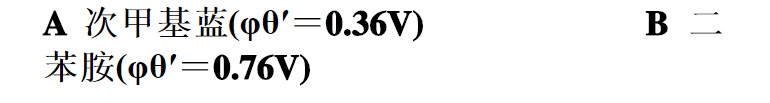
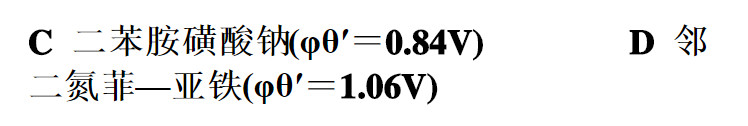
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在H3PO4存在下的HCl溶液中,用0.1mol/LK2Cr2O7溶液滴定0.1mol/L Fe2+溶液时,已知化学计量点的电位为0.86V。最合适的指示剂为( )。
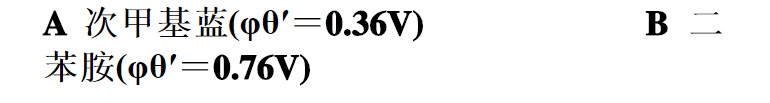
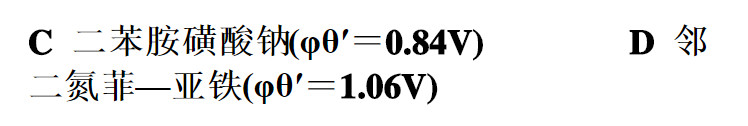
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在H3PO4存在下的HCl溶液中,用0.1mol/LK2Cr…”相关的问题
更多“在H3PO4存在下的HCl溶液中,用0.1mol/LK2Cr…”相关的问题
为测定HCl与H3PO4混合溶液中各钼分的浓度,取两份此试液。每份25.00mL,分别用0.2500mol·L-1NaOH标准溶液滴定,第一份用甲基橙为指示剂,消耗30.00mLNaOH标准溶液,第二份用酚酞为指示剂,消耗40.00mL。溶液中HCl与H3PO4的浓度关系是
A.C(H3P04)=c(HCl) B.c(H3PO4)=2c(HCl)
C.2c(H3PO4)=c(HCl)
A.#图片0$#
B.#图片1$#
C.#图片2$#
D.#图片3$#
某溶液中可能含下列物质的某些成分:H3PO4,NaH2PO4,Na2HPO4,HCl,取该溶液25.00cm3,甲基橙为指示剂,终点时用去0.2500mol·dm-3。NaOH溶液31.20cm3。另取25.00cm3试液,以酚酞为指示剂,终点时用去上述NaOH溶液42.34cm3。问该溶液含上述哪几种成分?浓度各为多少?
已知H3PO4的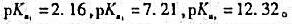 若用0.10mol/L的HCl溶液滴定0.10mol/L的Na3PO4溶液,则滴定到第二个化学计量点时体系的pH=()。
若用0.10mol/L的HCl溶液滴定0.10mol/L的Na3PO4溶液,则滴定到第二个化学计量点时体系的pH=()。
A.V1=V2
B.V1>V2
C.V1<V2
D.V1=2V2
E.V2=2V1
在NH3-NH4Cl缓冲溶液存在下(pH在10左右),用EDTA溶液滴定Zn2+,其滴定曲线突跃部分的长短主要与条件稳定常数的大小及金属离子的浓度有关,而与溶液中NH3的浓度大小无关。( )
HCl溶液回滴,用去3.25Ml.计算磷肥中有效P2O3的质量分数.
称取某试样1.000g,将其中的铵盐在催化剂存在下氧化为NO,NO再氧化为NO2,NO2溶于水后形成HNO3。此HNO3用0.01000mol/L NaOH溶液滴定,用去20.00mL。求试样中NH3的质量分数。(提示:NO2溶于水时,发生歧化反应3NO2+H2O→2HNO3+NO↑)