 更多“电池的电动势主要由电极与溶液间的相界电位、电极与导线间的接触…”相关的问题
更多“电池的电动势主要由电极与溶液间的相界电位、电极与导线间的接触…”相关的问题
第1题
若用pH玻璃电极与饱和甘汞电极组成电池,其电池电动势E与溶液pH间的关系可表示成E=K+0.059pH,试回
答: (1)该测量电池的表达式; (2)用直接读pH法测定时,要预先进行哪些调节?其目的何在?
点击查看答案
第2题
pH玻璃电极在使用时,必须浸泡24h左右,目的是()。
A.消除内外水化胶层与干玻璃层之间的两个扩散电位
B.减小玻璃膜和试液间的相界电位E内
C.减小玻璃膜和内参比液间的相界电位E外
D.减小不对称电位,使其趋于一个稳定值
第5题
准确量取30.00 mL弱酸HA,加水稀释至100.00 mL,在电池:(—)SHE|HA || SCE(+)中,以0.100 0 mol·L-1NaOH标准溶
准确量取30.00 mL弱酸HA,加水稀释至100.00 mL,在电池:(—)SHE|HA || SCE()中,以0.100 0 mol·L-1NaOH标准溶液滴定之。25℃时,当弱酸HA被中和一半时,电池电动势为0.524 V,化学计量点时,电池电动势为0.749 V。求:(1)弱酸HA的电离常数Kα值。(2)原弱酸HA溶液的浓度?(已知饱和甘汞电极的电极电位为0.244 V)
第7题
正离子选择性电极分析法中,()说法不正确。
A.参比电极电位恒定不变
B.待测离子价数愈高,测定误差愈大
C.指示电极电位与待测离子浓度呈斯特响应
D.电池电动势与待测离子浓度呈线性关系
第8题
用CLa(No3)3=0.03318mol?L-1的La(NO3)3溶液滴定100.0mL 0.03095mol?L-1的NaF的溶液,滴定反应为:
用CLa(No3)3=0.03318mol?L-1的La(NO3)3溶液滴定100.0mL 0.03095mol?L-1的NaF的溶液,滴定反应为:
 ,用固体LaF。膜电极为指示电极(正极),饱和甘汞电极为参比电极(负级),测得其滴定数据为:
,用固体LaF。膜电极为指示电极(正极),饱和甘汞电极为参比电极(负级),测得其滴定数据为:
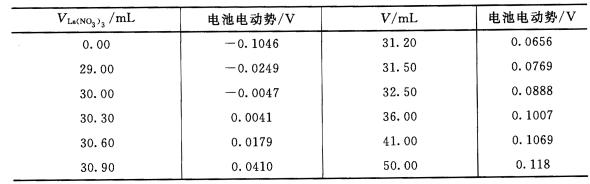 (1)计算反应完全时所需滴定剂的体积,并将其与电位滴定确定终点时消耗滴定剂的体积相比较。 (2)已知电池电动势与F一浓度的关系为:E=K+0.0592PF,用所测第一组数据算出K值。 (3)用求得的K值,计算加入50.00mI.,滴定剂后r的浓度?(设活度系数不变)
(1)计算反应完全时所需滴定剂的体积,并将其与电位滴定确定终点时消耗滴定剂的体积相比较。 (2)已知电池电动势与F一浓度的关系为:E=K+0.0592PF,用所测第一组数据算出K值。 (3)用求得的K值,计算加入50.00mI.,滴定剂后r的浓度?(设活度系数不变)
第10题
以下叙述正确的是______。
A.电极极化就是电极的电极电位偏离了由能斯特方程计算出来的平衡电位
B.原电池就是最原始的Cu-Zn电极组成的丹尼尔电池
C.电池的电动势为负值时就是原电池,否则就是电解池
D.可逆电极就是可以进行逆向电化学反应的电极


 如果结果不匹配,请
如果结果不匹配,请 

















