 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
写出下列反应方程式:(1)用氢气还原三氯化硼;(2)由三氟化硼和氢化铝锂制备乙硼烷:(3)由三氟化碉生成氟硼酸;(4)由三氯化确生成碉酸;(5)由硼的氧化物萤石、硫酸制取三氟化硼.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“写出下列反应方程式:(1)用氢气还原三氯化硼;(2)由三氟化…”相关的问题
更多“写出下列反应方程式:(1)用氢气还原三氯化硼;(2)由三氟化…”相关的问题
写出下列反应方程式。 (1)聚乙烯的氯化;(2)顺式一1,4一聚丁二烯的氯化;(3)醋酸纤维素;(4)硝基纤维素;(5)甲基纤维素;(6)聚乙烯的氯磺化。
把氯水滴加到Br-,I-混合液中的现象是先生成I2,I2被氧化成HIO3,最后生成Br2。
(1)写出有关的反应方程式。(2)有人说:“电动势大的反应一定先发生”。你认为如何?
案例:
下面是某化学老师关于“乙醇”的课堂教学片段。
【导入】表演魔术——魔棒点灯。这无根之火怎么产生的?我们先从这种液体研究起。
【学生活动】通过观察液体的颜色、状态、气味,得出结论,并试着在学案上写出乙醇的物理性质。
【投影】乙醇的物理性质
【探究l】根据信息提示,推测乙醇可能的结构。
经实验测定,乙醇的分子式为C2H60,且分子中每个碳原子可连接四个原子、每个氧原子可
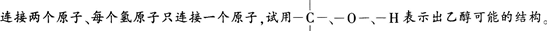
【学生活动】写出符合要求的可能结构。
【探究活动2】运用假设推理一实验验证一数据分析的方法确定乙醇的真实结构。【演示实验】乙醇与钠的反应并验证产物只有H:。
【思考与交流】由分子式C2H60推测,1 mol乙醇分子最多可提供——, mol氢原子参加反应,生成 ITIOl氢气分子。
【材料1】某化学兴趣小组关于“乙醇结构”的探究。
①量取2.9 mL的无水乙醇(约O.05 t001)于试管中,并加入足量的钠;②反应生成氢气体积标准状态为564 mL(约0.025 m01);
③通过讨论得出结论。【思考与交流】
①l tool乙醇实际生成了 mol氢气,mol氢原子。
②1个乙醇分子只能提供 个氢原子与Na反应生成氢气分子。
【追问】明明l个乙醇分子中含有6个氢原子,为什么却只能提供一个氢原子生成氢气呢?【学生活动】观察两种可能结构的球棍模型,根据这两种结构中氢所处位置的差异,确定乙醇的结构。
【师生互动】归纳乙醇的结构式、结构简式。
【对比】对比烧杯中钠与水、钠与乙醇的反应,根据钠与水反应的方程,尝试写出钠与乙醇的反应方程式。
乙醇与钠的反应实质:
CH3CH20H+Na→CH3CH20NaH2 ↑
【转引】从氧化还原的角度分析,乙醇在与钠的反应中做的是氧化剂,事实上,在大多数化学反应中.乙醇更愿意做还原剂。
【学生活动】根据有机反应方程式的书写规则,写出乙醇的燃烧方程式。
【探究3】材料一应用一实验探究乙醇的催化氧化反应。
【思考与交流】
①工厂高温焊接铜制器件时。表面生成黑的物质是什么?
②把发黑的铜制品趁热蘸一下酒精,就会恢复原有光泽,这又是什么原因。
【学生活动】根据桌上提供的仪器和药品,设计出合理的实验方案,通过实验,探究上述变化的可能原因。
【归纳总结】在铜或银作催化剂时,乙醇能被氧气氧化产生乙醛,我们称这个反应为乙醇的催化氧化反应。
问题:
(1)该教师在导入新课时,采用了哪种导入方法,并说明在教学实施过程中运用该导入法时应注意哪些问题。
(2)化学课堂上经常采用演示来完成教学,其构成要素及基本的类型有哪些?
(3)该教师在教学过程中,如何完成教学目标?
体;能与碳酸钠反应放出二氧化碳。写出该有机化合物的结构简式、名称及有关反应方程式。
化合物A的分子式为C6H14O,与金属钠作用放出氢气,与卢卡斯试剂作用可在数分钟后反应。A与浓H2SO4共热后的产物为B,B经酸性KMnO4氧化得到丙酸和丙酮两种产物。推测A、B的结构,并写出有关的化学反应方程式。
0mol/L的苯乙烯一二氯乙烷溶液在25℃下,用4.0×10-4mol/L的硫酸引发聚合,已知ktrM=1.2×10-1L/mol,kt1=6.7×10-3s-1(与反离子结合终止),kt2=4.9×10-2s-1(自发终止),Cs=0,Kp=7.6L/(mol.s)。 (1)写出链终止反应方程式,并计算产物的平均聚合度。 (2)在上述体系中再加入8.0×10-5mol/L异丙苯,写出链终止反应方程式,并求平均聚合度;Cs=4.5×10-2。 (3)比较上述两种情况的
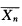 ,解释原因。
,解释原因。