 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在T=300K,反应A(g)+2B(g)=D(g)的K0=1。在一抽成真空的容器中,通入A,B,及D三种理想气体,在300K时,pA=pB=pD=100kPa,在此条件下,反应()
A、从右向左自动进行
B、反应处于平衡状态
C、从左向右自动进行
D、条件不全无法判断
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A、从右向左自动进行
B、反应处于平衡状态
C、从左向右自动进行
D、条件不全无法判断
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在T=300K,反应A(g)+2B(g)=D(g)的K0=1…”相关的问题
更多“在T=300K,反应A(g)+2B(g)=D(g)的K0=1…”相关的问题
A.向左进行
B.向右进行
C.处于平衡状态
D.无法确定
106J,请计算反应的Qp和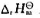 (WC,s,300K),已知C和w在300 K时的标准摩尔燃烧熔分别为-393.5kJ·mol-1和-837.5kJ·mol-1。
(WC,s,300K),已知C和w在300 K时的标准摩尔燃烧熔分别为-393.5kJ·mol-1和-837.5kJ·mol-1。
在300K时,反应2NOCl(g)=2NO+Cl2的NOCI浓度和反应速率的数据如下:

(1)写出反应速率方程式.
(2)求出反应速率常数.
(3)如果NOCl的起始浓度从0.30mol·dm-3增大到0.45mol·dm-3,反应速率将增大多少倍?
已知反应A(g)+2B(g)=2C(g)的△H>0,升高温度使v正增大,v逆减小,将导致平衡向右移动。( )
A.正、逆反应速率均减小
B.正反应速率减小;逆反应速率增大
C.正、逆反应速率均增大
D.正反应速率增大;逆反应速率减小
A.K不变,平衡不移动
B.K不变,平衡右移
C.K变大,平衡不移动
D.K变大,平衡右移
25℃,200kPa下,将4mol的纯A(g)放入带活塞的密闭容器中,达到如下化学平衡:
A(g)=2B(g).已知平衡时nA=1.697mol,nB=4.606mol.
(1)求该温度下反应的Kθ和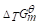 ;
;
(2)若总压为50kPa,求平衡时A,B的物质的量.
2
(g)达到平衡.此时,向反应系统中加入一定量的惰性组分H2O(g),则标准平衡常数Kθ(),C6H5C2H5(g)的平衡转化率α(),C6H5C2H3(g)的摩尔分数y(C6H5C2H3)().(选择填入:增大、减小、不变.)
nB=nB/nC=1,则此反应的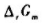 =();
=();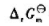 =();Kθ=().
=();Kθ=().