 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
浓度为4.12×10-5mol/L的1,10-邻二氮菲亚铁离子溶液用1.00cm的比色皿在波长508nm下测的吸光度为0.48。计算该溶液的摩尔吸光系数。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“浓度为4.12×10-5mol/L的1,10-邻二氮菲亚铁离…”相关的问题
更多“浓度为4.12×10-5mol/L的1,10-邻二氮菲亚铁离…”相关的问题
某有色物的浓度为1.0×10-5mol·L-1,以1.0cm吸收池在最大吸收波长下测得吸光度为0.280,在此波长下有色物的摩尔吸光系数为______L·mol-1·cm-1。
2.0mol/L苯乙烯的二氯乙烷溶液,于25℃时在4.0×10-4mol/L硫酸存在下聚合,计算开始时的聚合度。假如单体溶液中含有浓度为8.0×10-5mol/L的异丙苯,那么聚苯乙烯的聚合度是多少?为便于计算,可利用下列数据
。
5.(1)对于一个遵循米氏动力学的酶而言,当[S]=Km时,若V=35μmol/min,Vmax是多少μmol/min? (2)当[S]=2×10 -5mo/L,V=40μmol/min,这个酶的Km是多少? (3)若I表示竞争性抑制剂,KI=4×10-5mol/L,当[S]=3×10-2mol/L和[I]=3×10-5mol/L时,V是多少? (4)若I是非竞争性抑制剂,在KI、[S]和[I]条件与(3)中相同时,V是多少? (2)计算[S]=1.0×10-6mol/L和[S]=1.0×10-1mol/L时的v? (3)计算[S]=2.0×10-3mol/L或[S]=2.0×10-6mol/L时最初5min内的产物总量? (4)假如每一个反应体系中酶浓度增加到4倍时,Km,Vmax是多少?
A.4.24×10-10mol/L
B.4.24×10-5mol/L
C.4.24×10-10mol/L
D.1.34×10-5mol/L
A.5.29×10-4mol/L
B.5.29×10-5mol/L
C.1.67×10-5mol/L
D.1.67×10-4mol/L
25℃,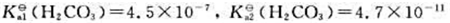 ,CO2饱和溶液的浓度为1.5×10-5mol·L-1,且假定溶于水中的CO2均生成了H2CO3试通过计算说明酸雨的pH应该小于多少?
,CO2饱和溶液的浓度为1.5×10-5mol·L-1,且假定溶于水中的CO2均生成了H2CO3试通过计算说明酸雨的pH应该小于多少?
A.4.12×10-4
B.8.4×10-15
C.7.1×10-15
D.1.7×10-7
A.氯化银沉淀溶解
B.不饱和溶液
C.C(Ag+)>(Cl-)
D.饱和溶液
[H+]=10-5mol/L的溶液,pH=______,[OH-]=10-2mol/L的溶液,pH=______。
0mol/L的苯乙烯一二氯乙烷溶液在25℃下,用4.0×10-4mol/L的硫酸引发聚合,已知ktrM=1.2×10-1L/mol,kt1=6.7×10-3s-1(与反离子结合终止),kt2=4.9×10-2s-1(自发终止),Cs=0,Kp=7.6L/(mol.s)。 (1)写出链终止反应方程式,并计算产物的平均聚合度。 (2)在上述体系中再加入8.0×10-5mol/L异丙苯,写出链终止反应方程式,并求平均聚合度;Cs=4.5×10-2。 (3)比较上述两种情况的
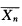 ,解释原因。
,解释原因。