 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在25℃,1mol/LHCl溶液中,用Fe3+标准溶液滴定Sn2+液。①计算滴定反应的平衡常数并判断
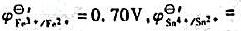 0.14V)
0.14V)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
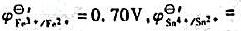 0.14V)
0.14V)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在25℃,1mol/LHCl溶液中,用Fe3+标准溶液滴定S…”相关的问题
更多“在25℃,1mol/LHCl溶液中,用Fe3+标准溶液滴定S…”相关的问题
用c(HCl)=0.1200mol/LHCl标准滴定溶液滴定含25%CaO、70%CaCO3、5%惰性杂质的混合物,若使HCl的用量在30mL左右,应称取试样多少克?
用K2Cr2O7标准滴定溶液在c(HCl)=1mol/L HCl溶液中滴定Fe2+,反应达化学计量点时的电位是1.02V,求此时Fe3+与Fe2+的浓度比。
称取土壤样品6.00g,用pH=7的1mol·dm-3醋酸铵提取,离心,转移含钙的澄清液于100cm3容量瓶中,并稀释至刻度。取50.00cm3该溶液在25℃时用钙离子选择性电极和SCE电极测得电动势为20.0mV,加入0.0100mol·dm-3的标准钙溶液1.0cm3,测得电动势为32.0mV,电极实测斜率为29.0mV,计算土壤样品中Ca2+的质量分数。
A.0.02~0.05mol/LHCl
B.2%NaOH水溶液
C.3%~5%HCl
D.NaHCO3水溶液
E.Ca(OH)2溶液
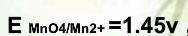 ,
,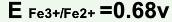 ,在此条件下用KMnO4标准溶液滴定Fe2+,其化学计量点时电位值是( )。
,在此条件下用KMnO4标准溶液滴定Fe2+,其化学计量点时电位值是( )。A.0.77V
B.1.06V
C.1.32V
D.1.45V
在1mol/L HCl溶液中,用Fe3+滴定Sn2-,计算下列滴定百分数时的电位:9%、50%、91%、99%、99.9%、100%、100.1%、101%、110%、200%。
称取Na2HPO4·12H2O试剂0.8835g,以甲基橙为指示剂,用0.1012mol/LHCl滴定至
计算BaSO4在2.0mol/LHCl溶液中的溶解度。已知BaSO4的Ksp=1.1×10-10,H2SO4的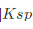 =1.2×10-2。
=1.2×10-2。