 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知反应BrO3-+5Br-+6H+﹦3Br2+3H2O,对Br-、BrO3-均为一级反应,对H+为二级反应,设该反应在酸性缓冲
溶液中进行,若向该反应体系加入等体积的含等浓度Br-的溶液,其速率变为原来的多少倍?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知反应BrO3-+5Br-+6H+﹦3Br2+3H2O,对…”相关的问题
更多“已知反应BrO3-+5Br-+6H+﹦3Br2+3H2O,对…”相关的问题
对于氧化还原反应BrO3-+5Br-+6H+====3Br2+3H2O。(1)求此反应的平衡常数;(2)计算当溶液的pH=7.0,[BrO3-]=0.10mol/L,[Br-]=0.70mol/L时,游离溴的平衡浓度。
(1)由附表六中查出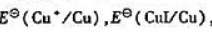 试计算
试计算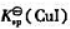 .
.
(2)计算298K下反应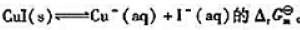
(3)若已知(2)中反应的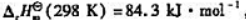 计算该反应的
计算该反应的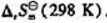
已知反应:
A+B→C+D1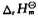 (T)=-40.0kJ·mol-1
(T)=-40.0kJ·mol-1
C+D→E1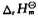 (T)=60.0kJ·mol-1
(T)=60.0kJ·mol-1
计算下列反应的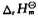 (T)。
(T)。
(1)C+D→A+B
(2)2C+2D→2A+2B ;
(3)A+B→E
A.2 :17
B.3 :5
C.4 :19
D.1 :3
(A) 1 (B) 2 (C) 3 (D) 0
已知下列原电池:
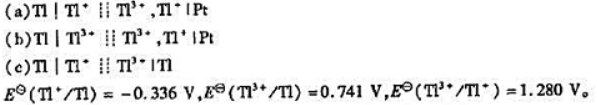
(1)写出各电池反应,并分别指出反应方程式中转移的电子数z;
(2)计算各电池的标准电动势EθMP;
(3)计算各电池反应的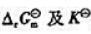 .
.
已知ϕθ(Cu2+/Cu+)=0.153V,ϕθ(I2/I-)=0.536V.
(1)计算ϕθ(Cu2+/CuI)的值.
(2)计算当c(Cu2+)=0.50mol·L-1,c(I-)=0.10mol·L-1时,反应2Cu2++4I-=2Cul+I2的标准平衡常数Kθ.
(3)判断在条件(2)下该反应的自发进行方向.[已知Kspθ(CuI)=1.27X10-12]