 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用Ox1滴定Red2,氧化还原反应为:电对的电极反应及电极电位分别为:试证明化学计量点的电
用Ox1滴定Red2,氧化还原反应为:
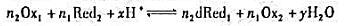
电对的电极反应及电极电位分别为:
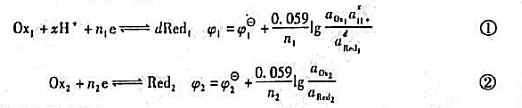
试证明化学计量点的电位为:
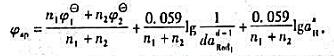
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
用Ox1滴定Red2,氧化还原反应为:
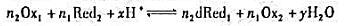
电对的电极反应及电极电位分别为:
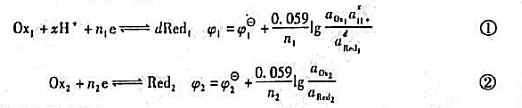
试证明化学计量点的电位为:
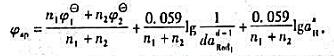
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“用Ox1滴定Red2,氧化还原反应为:电对的电极反应及电极电…”相关的问题
更多“用Ox1滴定Red2,氧化还原反应为:电对的电极反应及电极电…”相关的问题
A.凡是能进行氧化还原反应的物质,都能用直接法测定它的含量
B.酸碱滴定法是以质子传递反应为基础的一种滴定分析法
C.适用于直接滴定法的化学反应,必须是能定量完成的化学反应
D.反应速率快是滴定分析法必须具备的重要条件之一
E.按照所利用的化学反应不同,滴定分析法分为酸碱滴定法、氧化还原滴定法、配位滴定法、沉淀滴定法等四种方法
抗坏血酸(维生素C,摩尔质量为176.1g·mol-1)能被I2定量氧化,其反应为
C6H8O6+I2====C6H6O6+2HI
取100.0mL柠檬汁样品用H2SO4酸化,并加入20.00mL 0.02500mol·L-1I2溶液,待反应完全后,过量的I2用0.01000mol·L-1Na2S2O3标准溶液10.00mL滴定至终点,计算每毫升柠檬水果汁中抗坏血酸的质量。
在100.00 mL含亚砷酸盐的NaHCO3缓冲溶液中,用库仑滴定法电解产生I2来进行滴定,电极反应为
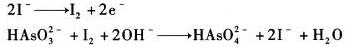 在1.00 mA的恒电流下经316 s达到终点,试计算试液中HASO32-的浓度?
在1.00 mA的恒电流下经316 s达到终点,试计算试液中HASO32-的浓度?
能适用于氧化还原滴定的反应(n1=n2=1),要求两电对的条件电极电位之差应大于______V。
在氧化还原滴定中,若氧化剂和还原剂两个半电池反应中,转移的电子数相等,即n1=n2,则计量点应在滴定突跃的______;若n1≠n2,则计量点偏向电子转移数______的电对一方。
拟定用氧化还原滴定法测定Ca2+的方案。要求写出测定原理、指示剂、操作步骤和含量计算公式。
A.滴定曲线是电流-滴定剂体积的关系图
B.滴定装置使用双铂电极系统
C.滴定过程存在可逆电对产生的电解电流的变化
D.要求滴定剂和被测物至少有一个为氧化还原电对
E.永停滴定法组成的是电解池
A.酸碱滴定法
B.沉淀滴定法
C.配位滴定法
D.氧化还原滴定法