 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
计算在pH=9.26氨性级冲溶液中,游离缓冲物质总浓度c(NH3-NH4+)=0.20mol·dm-3时Cu2+的aCukNH3值。
计算在pH=9.26氨性级冲溶液中,游离缓冲物质总浓度c(NH3-NH4+)=0.20mol·dm-3时Cu2+的aCukNH3值。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“计算在pH=9.26氨性级冲溶液中,游离缓冲物质总浓度c(N…”相关的问题
更多“计算在pH=9.26氨性级冲溶液中,游离缓冲物质总浓度c(N…”相关的问题
A.A、B两溶液 不相等
不相等
B.A、B两溶液 不相等
不相等
C.A、B两溶液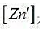 不相等
不相等
D.A、B两溶液[Zn2+]相等
·L-1HC1溶液后,溶液的pH有何变化?
(2)若在100mL pH=5. 00的HAe-NaAc级冲溶液中加入1.0mL,6.0mol·L-1NaOH后,溶液的pH增大0.10单位。问此级缓冲溶液中HAc、NaAc的分析浓度各为多少?
A.于pH=10的氨性缓冲溶液中直接加入三乙醇胺
B.于酸性溶液中加入KCN,然后调至pH=10
C.于酸性溶液中加入三乙醇胺,然后调至pH=10氨性溶液
D.加入三乙醇胺时不考虑溶液的酸碱性
E.以上方法都不行
计算在溶液中c(

A.两种情况下浓度相等
B.前者大于后者
C.后者大于前者
D.无法判断
E.以上都不正确

 ,试计算在c(H+)=1.0mol/L,c(
,试计算在c(H+)=1.0mol/L,c(


A.甲酸(pK=3.76)-Na0H
B.氨水(pK=4.74)-HCl
C.六亚甲基四胺(pK=8.85)-HCl
D.硼砂(pK=9.24)-HCl